LncRNAs在糖尿病及其并发症中的作用研究进展
时间:2023-06-22 16:45:04 来源:雅意学习网 本文已影响 人 
杨沁之 综述 罗茂 审校
西南医科大学:1.药学院药理系;2.药物研究中心(泸州 646000)
糖尿病是由于胰岛素分泌缺陷或生物作用受损所导致的血糖升高,可出现在生命的不同阶段,并导致多系统并发症。随着人类社会的进步及生活形式和饮食结构的改变,糖尿病病人数量急剧上升,成为全球增长最快的疾病之一[1]。据估计到2045年,18~99 岁的糖尿病病人数量将达到6.93亿[2]。长链非编码RNA(Long non-coding RNAs,LncRNAs)是一类缺乏蛋白质翻译能力的RNA 分子,由RNA 聚合酶Ⅱ转录所得,具有数量多、种类多的特点。虽然与蛋白编码基因相比,LncRNAs 的表达更低,但LncRNAs 细胞特异性相对较高[3]。近些年来的研究表明,LncRNAs不仅能通过多种机制的相互作用参与表观遗传修饰因子的招募、转录和转录后调控、mRNA 衰退的控制和转录因子的隔离等多种生物过程,并且在肿瘤、心脏病和糖尿病等疾病的病理进程中起着关键作用[4]。如今随着研究的深入,研究人员发现LncRNAs 在糖尿病中功能异常,影响特定的LncRNAs的表达能调控糖尿病及其并发症的病理发展过程[5-7]。本文主要就LncRNAs 在糖尿病及其并发症中的作用最新研究进展作一综述,以期为糖尿病及其并发症的研究和医治提供理论依据。
LncRNAs 是20 世纪末期被发现的一类具有特定功能的调控RNA,广泛参与细胞代谢的各个领域。目前对LncRNAs的分类是基于它们的结构或大小、定位、功能以及与其他组件的相互作用。有研究表明,这些LncRNAs 大多来自基因组的基因间、外显子或远端蛋白编码区等非保守区,在进化中更易发生快速的翻新[8-9]。依据基因组中LncRNAs 所处的位置及背景,大致可将其分为正义LncRNAs、反义LncRNAs、双向Ln⁃cRNAs、内含子LncRNAs和基因间LncRNAs五类[10]。
随着分子生物技术的持续发展,LncRNAs 的效应机制逐渐浮出水面,越来越多的研究发现,LncRNAs可通过与DNA/RNA结合或与蛋白结合在多种生理、病理过程发挥重要作用,其中包括参与基因表达、基因组印迹、核与胞质间囊泡运输、RNA 编辑、翻译等过程的调控[11]。另外,LncRNAs 具有顺式(cis-)或反式调节(trans-regulation),其顺式调节对临近基因发挥作用,而反式调节则对远离其转录位点的基因发挥作用。尽管目前对LncRNAs 功能的了解还只是冰山一角,但是越来越多的证据显示其在X 染色体失活、细胞周期调控、分化和凋亡等细胞生命进程中发挥着重要的作用[12]。近年来,LncRNAs 在各种疾病的研究中获得了显著成就,并且在不同类型糖尿病中的关键调节作用也逐渐被广泛报道[13]。因此,对LncRNAs 在糖尿病中的功能作用展开进一步的探索是非常有必要的。
在机体中,胰岛分泌胰岛素调节血糖浓度,肝脏和肌肉储存糖原,另外多余的葡萄糖则转化为脂肪而囤积起来。糖尿病分为1 型糖尿病(type 1 diabetes,T1DM)、2 型糖尿病(type 2 diabetes,T2DM)、妊娠期糖尿病及其他类型或称继发性糖尿病。虽然定义糖尿病表型的潜在原因极其复杂,但是过去几十年的研究主要集中在蛋白质编码基因上。LncRNAs作为近几年生物学领域的研究热点之一,正在成为控制代谢组织发育和功能的重要调控元件[14]。近年来研究表明,一些LncRNAs 参与调控胰岛发育、肝脏代谢、肌肉再生和脂肪细胞分化,在葡萄糖和脂质代谢中发挥着重要作用,本文依据LncRNAs 在不同代谢组织的作用,绘制了糖尿病代谢组织中LncRNAs的示意图[15-37],见图1。下面就LncRNAs在关键代谢组织中的代谢稳态调控作用展开论述,见表1。

图1 糖尿病不同代谢组织中的LncRNAsFigure 1 LncRNAs in different metabolic tissues of diabetes mellitus
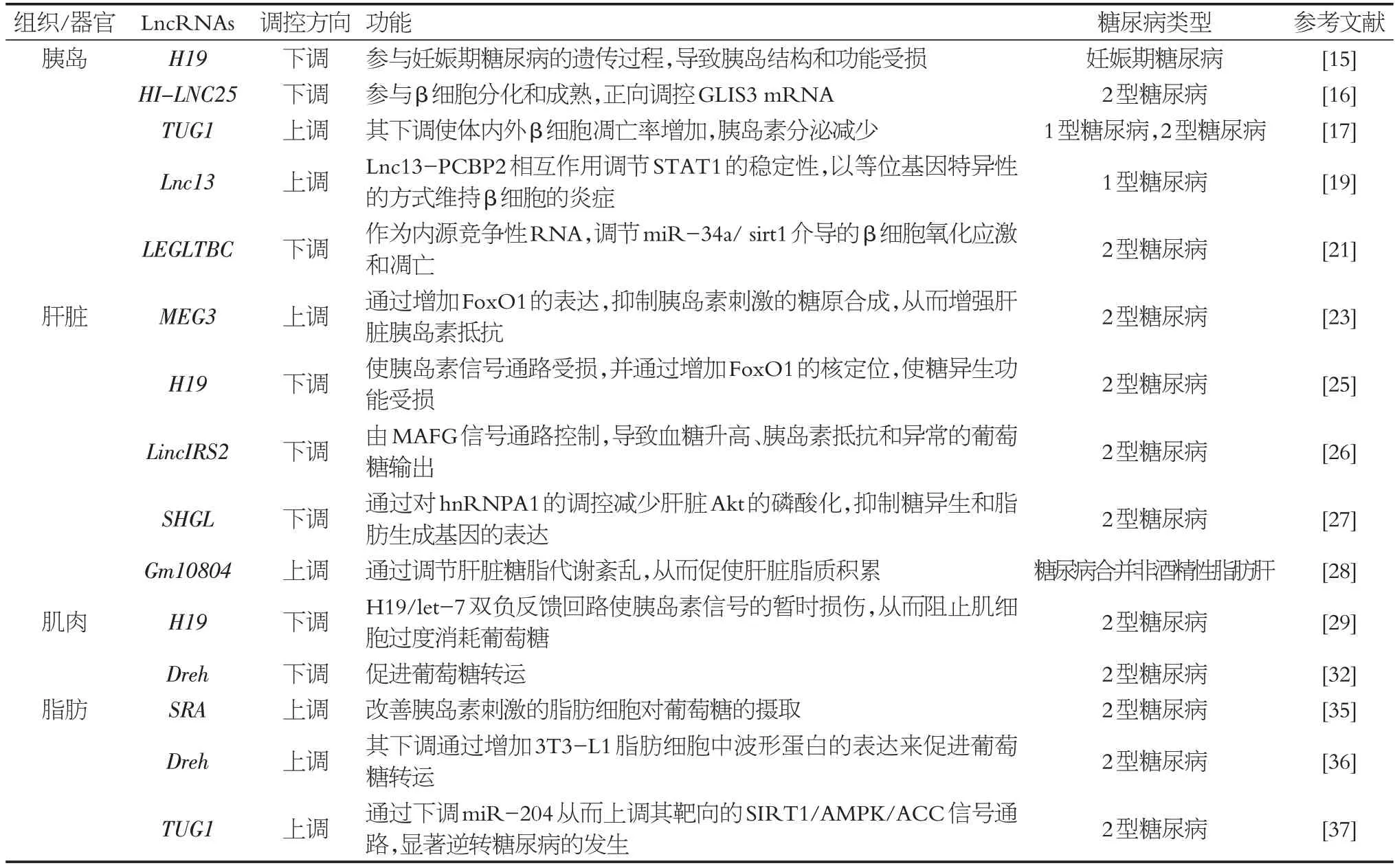
表1 与糖尿病相关的LncRNAsTable 1 LncRNAs associated with diabetes
2.1 LncRNAs与胰岛
胰脏分为胰腺和胰岛两部分,同时具有内分泌和外分泌的功能。胰腺负责感知血液里葡萄糖水平,而胰岛β 细胞分泌胰岛素,以刺激外周组织对葡萄糖的吸收。其中胰岛是研究人员了解糖尿病病理生理的重要中枢节点。在T1DM中,胰岛β细胞的丧失和胰岛素分泌不足促使血糖升高[38-39];
在T2DM中,高血糖由β细胞功能障碍和胰岛素抵抗引起[40],而胰岛素抵抗时,机体将无法对正常胰岛素水平做出反馈。DING等[15]首先证明了LncRNAs具有对胰岛发育和功能调控的可能,其中LncRNA H19参与了妊娠期糖尿病的遗传过程,导致胰岛超微结构和功能受损。此外,MORÁN I等[16]通过对2型糖尿病患者胰腺β细胞的高通量测序,发现了具有组织特异性和动态调节的异常表达的Ln⁃cRNAs。这些LncRNAs通常位于含有胰岛特异编码基因的胰岛特异染色质结构域附近,或者定位于糖尿病易感基因位点。其中HI-LNC25是一种在小鼠和人之间保守的β细胞特异性LncRNAs,它的下调导致GLIS3(一个重要的胰岛转录因子)的降低,提示其在胰岛β细胞中的功能重要性。YIN等[17]发现沉默LncRNA 牛磺酸上调基因1(taurine-upregulated gene 1,TUG1)会诱导MIN6细胞和胰腺β细胞的凋亡,减少胰岛素的分泌,从而导致空腹血糖水平升高。同样,LncRNA 母系印记基因3(maternally expressed gene 3,Meg3)也被证明可以调节胰岛素分泌和β 细胞凋亡。在T1D 和T2D小鼠模型[分别为非肥胖糖尿病(non-obese diabetic,NOD)和高血糖db/db 小鼠] 的胰岛中Meg3的表达下调,同时ins2、Pdx1和Mafa的水平显著降低[18]。Pdx-1是一种关键的β细胞转录因子,与胰岛素合成和β细胞特异性调控网络有关。除此之外,有研究报道Ln⁃cRNAs 在β 细胞功能中的作用可能是普遍的[41],对其进行深入探索可能有助于恢复糖尿病引起的代谢紊乱。
2.2 LncRNAs与肝脏
肝脏是许多代谢过程的场所,能同时利用和产生葡萄糖,对LncRNAs 与肝脏关系的理解有利于进一步探究LncRNAs与糖尿病之间的联系。肝脏特异性甘油三酯调节因子(Lnc liver-specific triglyceride regulator,LncLSTR)是一种肝脏特异性LncRNA,调节全身脂质代谢,LI等[22]发现其水平降低对小鼠有显著的降脂作用,且与小鼠甘油三酯(triglycerides,TG)的清除增强有关。在此过程中,LncSTR与TDP-43结合形成复合体,通过调节Cyp8b1 的活性改变影响法尼醇X 受体(frne⁃soid X receptor,FXR)途径的胆汁酸水平,从而增强肝脏中甘油三酯的清除。因此,LncLSTR 等肝脏富集的LncRNA 可能为糖尿病高脂血症患者提供新的治疗策略。此外,有研究发现在高脂饮食(high-fat diet,HFD)小鼠、ob/ob 小鼠和经棕榈酸盐、油酸盐或亚油酸盐处理的原代肝细胞中,肝脏LncRNA MEG3水平的升高与G6pc、Pepck、FoxO1表达的增加有关[23]。该实验最终使肝脏糖异生的增加以及肝细胞中受胰岛素刺激的糖原积累受损,其表现为肝胰岛素抵抗。然而,当干预高脂饮食和ob/ob 小鼠的MEG3时,可显著减轻受损的糖耐量,提示LncRNA MEG3在肝脏中对葡萄糖的调控作用。另一种禁食诱导的LncRNA,肝脏葡萄糖激酶抑制因子(liver glucokinase repressor,LGR),可通过与hnRNPL相互作用抑制葡萄糖激酶活性,并抑制小鼠肝脏中糖原的储存[24]。GOYAL等[25]研究显示在db/db 小鼠肝脏中,可调节肝脏的糖异生的H19水平明显降低。并且当人肝癌和原代肝细胞中的H19沉默时会增加糖异生基因的水平和肝脏葡萄糖产量。另外H19还与肝脏发育及其他肝病的进展有关。综上所述,糖尿病患者常有肝脏代谢功能障碍,因此有必要了解LncRNAs 在肝脏病理中的作用机制。
2.3 LncRNAs与肌肉
在糖、脂代谢的过程中,肌肉细胞通过糖酵解增加对的血糖的利用,在葡萄糖代谢中同样起着重要作用。近年,GAO等[29]发现肌肉细胞的葡萄糖代谢与H19/let-7双负反馈回路密切相关。该研究发现LncRNA-H19在糖尿病受试者和小鼠骨骼肌的表达量明显下降,并且在损害胰岛素信号传导和降低葡萄糖摄取方面起着重要作用。此外LncRNAs也是参与肌肉分化和再生的重要调节因子。其中与MyoD 活性相关的LncRNAs 与肌原分化至关重要。据报道MyoD 能至少诱导Linc-RAM和Dum两个LncRNAs 的转录。其中Linc-RAM与MyoD结合,并共同与两个重要的核小体重构体BAF60c和BRG1等染色质修饰剂相互作用。在分化过程中,核糖核酸复合物以肌原基因为靶点,以适当协调基因表达[30]。LncRNA-Dum通过招募DNA 甲基化蛋白,使其邻近基因发育多能性相关2(developmental pluripotency-associated 2,Dppa2)沉默,从而调控肌发生[31]。
2.4 LncRNAs与脂肪
在肝脏和肌肉中,葡萄糖分别会被储存为肝糖原和肌糖原,而更多的葡萄糖会在胰岛素的帮助下转化为脂肪囤积起来。此外脂肪细胞能产生具有关键代谢功能的关键脂肪因子。在肥胖患者中,巨噬细胞的聚集以及脂肪炎症增加可能导致胰岛素抵抗、T2D 和代谢综合征。有研究通过高通量测序技术,发现大量的LncRNAs 在脂肪细胞分化和成熟过程差异表达,足以证明LncRNAs 在脂肪组织发育过程中的重要作用[42]。另外的研究同样发现LncRNA-Blnc1能与转录因子Ebf2 相互作用以调节产热基因的调控程序,从而调节棕色脂肪细胞的发育[33]。与腹部脂肪相比,LncRNA-HOTAIR在臀部脂肪细胞中差异表达,并在脂肪细胞分化中发挥作用[34]。LncRNAs 对于脂肪的影响,除了参与脂肪分化,还可以影响动物的生理状态。类固醇受体RNA 激活剂(steroid receptor RNA activator,SRA)是一种在脂肪组织中高表达的长链非编码RNA,能共同激活类固醇受体依赖报告基因的表达,促进脂肪生成。在构建小鼠模型中,SRA 基因敲除显示出更强的胰岛素敏感性,并通过改善糖耐量抵抗饮食诱导的肥胖[35]。总之,探讨LncRNAs在脂肪组织中的作用关系,可能为糖尿病脂质代谢紊乱机制的研究提供新的思路。
糖尿病的高血糖状态促进了微血管和大血管并发症的产生,从而导致糖尿病患者死亡率增加以及整体生活质量下降。糖尿病肾病(diabetic nephropathy,DN)与视网膜病(diabetic retinopathy,DR)被并列为糖尿病性微小血管病变的代表,二者密切相关,往往在临床上见于同一个糖尿病的患者,使患者苦不堪言[43]。此外,据调查,70%的糖尿病患者死于心血管疾病(cardiovas⁃cular disease,CVD),糖尿病患者心血管疾病目前仍然是1 型或2 型糖尿病患者高发病率和死亡率的主要原因[44-45]。如前所述,LncRNAs 除了参与糖尿病期间的主要代谢组织外,还与糖尿病并发症有关。因此,了解LncRNAs在糖尿病并发症中的作用机制对将来该病的防治有重要意义。
3.1 LncRNAs与糖尿病肾病
糖尿病肾病是糖尿病最有害的微血管并发症,也是终末期慢性肾病的主要病因。细胞外基质(extracel⁃lular matrix,ECM)的积聚,使多数肾细胞纤维化增加,是糖尿病肾病的一个主要特征[46]。近年研究发现,在肾脏多种细胞中高表达的LncRNA 浆细胞瘤变体易位1(the plasmacytoma variant translocation1,PVT1)与这一进程有关。ALVAREZ等[47]通过RNA 干扰技术敲除肾小球系膜细胞的PVT1基因,发现经高糖处理后的人系膜细胞中PVT1的表达显著上调;
沉默PVT1后细胞外基质中的基因和蛋白水平显著降低,提示LncRNAs 在糖尿病肾病中扮演着重要角色。另外研究发现特定的LncRNAs 能干扰糖尿病肾病相关的炎症过程。LncRNA-Gm4419是一种调节NF-JB/NLRP3 炎症小体活性的LncRNA,可与肾小球系膜细胞中的炎症因子相互作用;
Gm4419敲除可降低细胞增殖并抑制其在高血糖状态下NF-κB 的表达[48],提示LncRNAs 能经过炎症相关信号通路介入糖尿病肾病中的炎症和纤维化过程。
3.2 LncRNAs与糖尿病视网膜病
糖尿病视网膜病是一种影响视网膜神经元和微血管系统的疾病,可导致糖尿病患者视力受损或丧失。据报道,LncRNA-MALAT1和MEG3均与糖尿病视网膜病变有关。YAN B等[49]建立链脲霉素(streptozotocin,STZ)诱导的糖尿病小鼠模型,通过微阵列分析发现Ln⁃cRNAs 在糖尿病小鼠视网膜上的显著上调,而敲除MALAT1可减轻STZ 诱导的大鼠视网膜病变。最近也有研究显示,LncRNA-MALAT1通过Keap1-Nrf2调节糖尿病视网膜病变中的抗氧化防御,抑制MALAT1能保护视网膜免受氧化损伤[50]。上述结果表明LncRNAs参与DR 的病理进程,并且LncRNA-MALAT1具有预防或减缓糖尿病视网膜病变的潜力。另外LncRNA MEG3在STZ诱导的糖尿病小鼠的视网膜中也被发现下调,其在视网膜内皮细胞中的体外敲除被发现调节细胞的增殖、活性和迁移[51]。除此之外,已有多项研究证实Ln⁃cRNAs参与了糖尿病视网膜病变的发病过程[52-55]。
3.3 LncRNAs与糖尿病心血管疾病
心血管疾病研究表明LncRNAs参与多种心血管疾病发生发展,包括心肌梗塞(myocardial infarction,MI)、心肌肥大、冠心病(coronary heart disease,CHD)、动脉粥样硬化以及心力衰竭(heart failure,HF)等[56]。LEUNG等[57]研究发现Lnc-Ang362在血管平滑肌细胞中被血管紧张素II 信号上调。Lnc-Ang362是mir-221和mir-222的宿主RNA,这两个miRNAs 参与血管平滑肌细胞的增殖。因此,诱导Lnc-Ang362会导致miR⁃NAs表达上调,促进细胞增殖,提示LncRNAs与血管细胞、功能的相关性。LncRNA-SRA在不同类型的人类疾病中发挥着关键作用,此前已经提到LncRNA-SRA可以抑制脂肪甘油三酯脂肪酶的表达。近年来也有报道称LncRNA-SRA有助于血管平滑肌细胞(vascular smooth muscle cells,VSMCs)的增殖,在心血管疾病的病理进程中起着关键作用。REN等[58]对糖尿病心血管疾病的五年随访研究发现LncRNA-SRA在糖尿病合并心血管疾病患者中特异性下调,并且通过调节VSMCs 的生存能力参与糖尿病心血管疾病的发病机制。因此,血浆LncRNA-SRA可能作为一种潜在的生物标志物,为糖尿病心血管疾病的诊断和预后提供新的参考指标。
糖尿病的病因和发病机制极其复杂,至今仍有许多疑问需要解答。近来的研究表明,LncRNAs 的表达和功能的失调反映了多种病理生理状态,同时也参与了糖尿病的发生与发展。一方面,异常表达的Ln⁃cRNAs参与细胞组织生命活动,影响糖类、脂肪等营养物质的正常代谢;
另一方面,某些LncRNAs的抑制能有效缓解糖尿病及其并发症的部分症状。目前已有不少LncRNAs 被鉴定出具有诊断和治疗各种疾病的潜力。在体液中,LncRNAs 能够抵抗核糖核酸酶的作用而具有高度稳定性[59],再加上它们模仿疾病进展的表达模式,使其成为理想的生物标记物候选者。另外,Ln⁃cRNAs 因其在调节细胞通路方面的特异性功能,将可能成为更好的治疗靶点。因此,LncRNAs 在糖尿病及其并发症的诊断、预防和治疗中具有非常好的前景,有望被应用于临床。随着对糖尿病的不断了解,期望未来发现更多LncRNAs在糖尿病及其并发症发病过程中所起的作用。
(利益冲突:无)
猜你喜欢胰岛葡萄糖调节方便调节的课桌青少年科技博览(中学版)(2022年11期)2023-01-07临床胰岛制备研究进展医学信息(2022年9期)2022-11-272016年奔驰E260L主驾驶座椅不能调节汽车维修与保养(2021年8期)2021-02-16葡萄糖漫反射三级近红外光谱研究中国甜菜糖业(2020年1期)2020-12-07糖耐量试验对葡萄糖用量的要求江苏卫生保健(2018年7期)2018-07-31葡萄糖对Lactobacillus casei KDL22发酵及贮藏性能的影响中国乳业(2016年4期)2016-11-07可调节、可替换的takumi钢笔工业设计(2016年4期)2016-05-041型糖尿病小鼠胰岛微血管内皮细胞超微结构受损中国病理生理杂志(2015年8期)2015-12-21多发性肺硬化性血管瘤18~F-脱氧葡萄糖PET/CT显像1例肿瘤影像学(2015年3期)2015-12-09非编码RNA在胰岛发育和胰岛功能中的作用中国医学科学院学报(2014年6期)2014-03-11







