一测多评法测定槐花颗粒中7种有效成分含量
时间:2023-06-13 12:55:15 来源:雅意学习网 本文已影响 人 
辛晓芳,刘特津,张公安
(1.广州中医药大学附属中山中医院,广东 中山 528401;
2.广东药科大学,广东 中山 528458)
槐花颗粒为广东省中山市中医院的院内制剂,由槐花、野菊花、甘草组成,具有凉血止血、清肝泻火的功效,主要用于治疗便血、痔血、血痢、崩漏、吐血、肝热目赤、头痛、眩晕等,临床疗效显著。槐花颗粒目前的质量标准过于简单,无法全面反映和控制产品的质量。一测多评法(quantitative analysis of multi-components by single-marker,QAMS)已广泛应用于中药及复方制剂的质控研究[1-4],通过中药有效成分内在函数关系和比例关系,以药材中对照品廉价易得的典型成分为内标,建立该成分与其他成分间的相对校正因子,再通过校正因子同步计算出其他成分的量,从而实现多成分的同步测定。为了提高制剂质量,本研究采用一测多评法建立槐花颗粒的多成分质控模式,为该制剂的质量控制提供科学依据。
1.1 仪器Agilent 1260高效液相色谱仪(美国安捷伦科技有限公司);
Waterse 2695高效液相色谱仪[沃特世科技(上海)有限公司];
色谱柱Agilent ZORBAX Eclipse XDB-C18(4.6 mm×250 mm,5 μm,美国安捷伦科技有限公司);
色谱柱Agilent ZORBAX RX-C18(4.6 mm×250 mm,5 μm,美国安捷伦科技有限公司);
色谱柱Agilent ZORBAX SB-C18(4.6 mm×250 mm,5 μm,美国安捷伦科技有限公司);
色谱柱Merck Purospher STARRP-18 endcapped(4.6 mm×250 mm,5 μm,德国默克公司);
医用离心机2-16R(湖南恒诺仪器设备有限公司);
SQP型Sartorius天平[赛多利斯科学仪器(北京)有限公司]。
1.2 试药对照品绿原酸(批号110753-202018)、芦丁(批号100080-201811)、甘草苷(批号111610-201908)、木犀草苷(批号111720-201810)、蒙花苷(批号111528-201911)、木犀草素(批号111520-202006)、槲皮素(批号100081-201610),均购于中国药品生物制品检定所;
乙腈(色谱纯),甲醇(分析纯);
槐花颗粒(粤 药 制 备 字Z20200038000,批 号20001、20002、20003、20004、21001、21002),由广东省中山市中医院制剂室提供。
2.1 混合对照品溶液的制备分别精密称取绿原酸、芦丁、甘草苷、木犀草苷、蒙花苷、槲皮素、木犀草素对照品适量,加甲醇溶解并定容至50 ml,制成质量浓度分别 为0.021 0 mg/ml、0.450 0 mg/ml、0.210 0 mg/ml、0.020 0 mg/ml、0.092 5 mg/ml、0.212 5 mg/ml、0.075 0 mg/ml的混合对照品储备液,用封口膜封口并避光保存。
2.2 供试品溶液的制备取同一批号的槐花颗粒5 g,加入70%乙醇(固液比1∶20)在80℃水浴中加热,索氏提取法抽提4 h,待提取液冷却后过滤,除去提取液中的药材粉末,分批将滤液置于同一蒸发皿中水浴蒸干,残渣加甲醇溶解,转移到棕色容量瓶中并定容至50 ml,取定容后的试液少许,以转速13 500 r/min离心15 min,取上清液1 ml置于10 ml棕色容量瓶中,加甲醇定容至刻度,即得供试品溶液,用封口膜封口并避光保存。
2.3 阴性溶液的制备按槐花颗粒制剂的配制工艺分别制成缺槐花、缺野菊花、缺甘草的阴性颗粒。然后按上述2.2提取方法,分别制备出甘草阴性样品溶液、槐花阴性样品溶液、野菊花阴性样品溶液。
2.4 色谱条件色谱柱:Agilent ZORBAX Eclipse XDB-C18(4.6 mm×250 mm,5 μm);
流动相:乙腈(A)-0.5%磷酸水溶液(B),梯度洗脱程序为:0~20 min,10%~19%乙腈洗脱;
20~30 min,19%~20%乙腈洗脱;
30~50 min,20%~21%乙腈洗脱;
50~85 min,21%~60%乙腈洗脱;
85~95 min,10%乙腈洗脱;
流速:1.0 ml/min;
检测波长:334 nm;
柱温:25℃;
进样量:5 μl。在上述色谱条件下,混合对照品和供试品中绿原酸、芦丁、甘草苷、木犀草苷、蒙花苷、槲皮素、木犀草素分离良好,且芦丁峰的理论塔板数不低于3 000。见图1。

图1 HPLC色谱图
2.5 方法学考察
2.5.1 线性关系考察分别精密吸取“2.1”项下混合对照品储备液各1.0 ml、2.0 ml、4.0 ml、6.0 ml、8.0 ml于10 ml量瓶中,用甲醇稀释并定容,制得系列混合对照品溶液。将系列混合对照品溶液及混合对照品储备液,在“2.4”项色谱条件下测定其峰面积。以混合对照品溶液的浓度为横坐标(X,μg/ml),测得的峰面积为纵坐标(Y),绘制标准曲线,得回归方程及相关系数r²,结果r²均大于0.999,显示进样浓度与峰面积呈良好线性关系,结果见表1。

表1 槐花颗粒中7种成分的线性关系考察结果
2.5.2 精密性试验取“2.1”项下混合对照品溶液,按“2.4”项下色谱条件连续进样6次,记录峰面积,结果显示绿原酸、芦丁、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的峰面积相对标准偏差(RSD)依次为1.03%、0.99%、1.03%、1.03%、1.03%、1.02%、1.03%(n=6),表明仪器精密度良好。
2.5.3 重复性试验取同一批供试品(批号20004)6份,按“2.2”项下方法平行制备供试品溶液6份,再按“2.4”项下色谱条件依次进样测定,计算绿原酸、芦丁、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的浓度分别为7.8 μg/ml、329.5 μg/ml、71.2 μg/ml、6.9 μg/ml、41.1 μg/ml、6.4 μg/ml、47.1 μg/ml,RSD分别为1.00%、1.03%、1.02%、1.03%、1.00%、1.02%、1.00%(n=6),表明方法重复性良好。
2.5.4 稳定性试验取同一批供试品(批号20004),按“2.2”项下方法制备供试品溶液,室温下放置,分别在0 h、4 h、8 h、12 h、16 h、20 h、24 h测定,记录峰面积,结果绿原酸、芦丁、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的峰面积RSD依次为1.03%、1.03%、1.04%、1.04%、1.00%、1.01%、1.04%(n=6),表明供试品溶液在24 h内稳定性良好。
2.5.5 加样回收率试验分别精密称取绿原酸、芦丁、甘草苷、木犀草苷、蒙花苷、槲皮素、木犀草素对照品适量,加甲醇溶解并定容至10 ml,制成质量浓度分 别 为1.950 mg/ml、65.016 mg/ml、15.080 mg/ml、1.740 mg/ml、9.500 mg/ml、1.506 mg/ml、10.500 mg/ml的混合对照品溶液。精密称定9份已测定的槐花颗粒样品(批号20004)2.5 g,分为低、中、高3组(分别加入0.8 ml、1.0 ml、1.2 ml的混合对照品溶液),每组平行制备3份,按“2.2”项下方法制备供试品溶液,再按“2.4”项下色谱条件进行测定,分别计算绿原酸、芦丁、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的平均回收率,各成分平均回收率分别为98.89%、98.69%、98.49%、98.11%、98.21%、98.33%、98.30%,RSD依次为1.53%、0.98%、0.69%、0.88%、1.37%、0.62%、0.81%(n=9),表明该方法的准确性良好。
2.6 QAMS法
2.6.1 相对校正因子(fS/I)的测定取“2.5.1”项数据,以芦丁为内参物(S),按公式fS/I=(AS×CI)/(AI×CS)计算,AI、CI分别为待测成分对照品的峰面积和质量浓度,AS、CS分别代表内参物的峰面积和质量浓度。计算绿原酸、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的相对校正因子fS/A、fS/B、fS/C、fS/D、fS/E、fS/F的RSD分别为1.73%、2.71%、2.45%、2.26%、2.53%、1.64%,结果见表2。

表2 以芦丁为内参物的fS/I测定结果
2.6.2 相对校正因子重现性考察
2.6.2.1 不同仪器对fS/I的影响试验考察了2种高效液相色谱系统Agilent 1 260高效液相色谱仪和Waterse 2 695高效液相色谱仪对槐花颗粒中6种有效成分绿原酸、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的相对校正因子fS/A、fS/B、fS/C、fS/D、fS/E、fS/F的影响,结果显示RSD依次为1.47%、1.19%、1.26%、0.65%、1.38%、0.73%,结果见表3。表明不同仪器对各成分的fS/I无显著性差异。

表3 不同仪器对fS/I的影响
2.6.2.2 不同色谱柱对fS/I的影响试验考察了4种色谱柱Merck Purospher STARRP-18 endcapped、Agilent ZORBAX Eclipse XDB-C18、Agilent ZORBAX RX-C18、Agilent ZORBAX SB-C18对槐花颗粒中6种有效成分绿原酸、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的相对校正因子fS/A、fS/B、fS/C、fS/D、fS/E、fS/F的影响,结果显示RSD依次为1.00%、1.61%、1.99%、0.79%、1.94%、0.42%,结果见表4。表明不同色谱柱对各成分的fS/I无显著性差异。
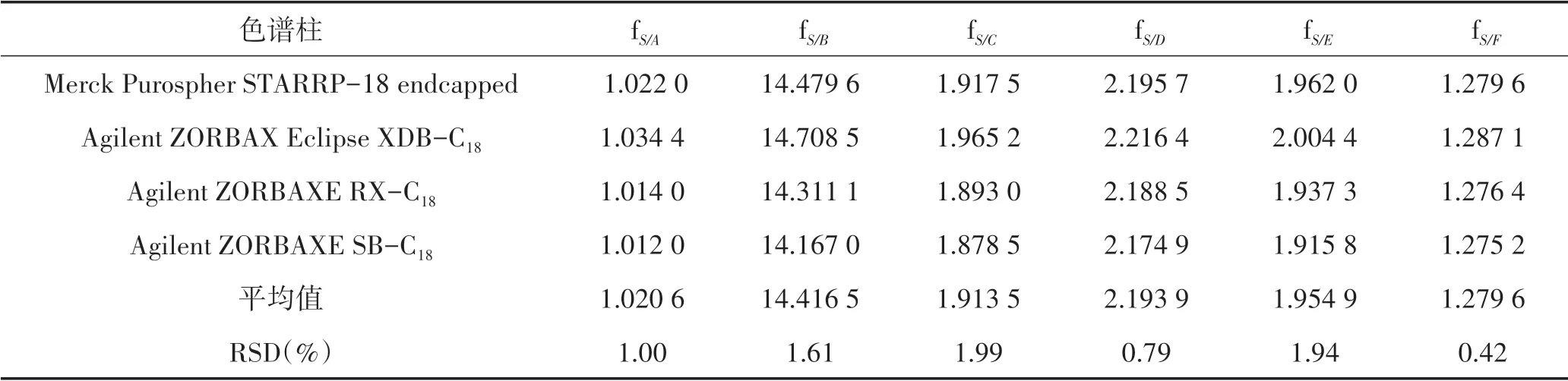
表4 不同色谱柱对fS/I的影响
2.6.2.3 不同柱温对fS/I的影响试验考察了同一色谱柱(Agilent ZORBAX Eclipse XDB-C18)不 同 柱 温(20℃、25℃、30℃、35℃)对槐花颗粒中6种有效成分绿原酸、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的相对校正因子fS/A、fS/B、fS/C、fS/D、fS/E、fS/F的影响,结果显示RSD依次为0.88%、0.77%、1.20%、0.39%、1.16%、0.66%,结果见表5。表明不同柱温对各成分的fS/I无显著性差异。

表5 不同柱温对fS/I的影响
2.6.2.4 不同操作人员对fS/I的影响试验考察了3名试验人员对槐花颗粒中6种有效成分绿原酸、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的相对校正因子fS/A、fS/B、fS/C、fS/D、fS/E、fS/F的影响,结果显示RSD依次为0.50%、0.63%、0.98%、0.39%、1.18%、0.23%,结果见表6。表明不同试验人员对各成分的fS/I无显著性差异。

表6 不同试验人员对fS/I的影响
2.6.2.5 不同流速对fS/I的影响试验考察了3种流速(0.8 ml/min、1 ml/min、1.2 ml/min)对槐花颗粒中6种有效成分绿原酸、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的相对校正因子fS/A、fS/B、fS/C、fS/D、fS/E、fS/F的影响,结果显 示RSD依 次 为0.80%、1.39%、0.92%、0.39%、1.21%、0.33%,结果见表7。表明不同流速对各成分的fS/I无显著性差异。
2.6.3 色谱峰定位参数考察利用相对保留时间(rI/S)进行峰定位,r(I/S)=tR(I)/tR(S)(注:I为待测成分,S为内参物),测得绿原酸、芦丁、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素的相对保留时间(rI/S)的结果,见表8。不同色谱条件所的到相对保留值变动较小,rA/S、rB/S、rC/S、rD/S、rE/S、rF/S的RSD(%)均<2%,表明采用rI/S对绿原酸、芦丁、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素进行色谱峰的定位良好。

表8 不同仪器和色谱柱测得的相对保留时间
2.6.4 QAMS法与外标法测定结果比较取6批次的样品,按“2.2”项下方法制备供试品溶液,并按“2.4”项下色谱条件进样,记录峰面积,分别采用外标法和QAMS法计算各批次样品中绿原酸、芦丁、甘草苷、木犀草苷、蒙花苷、木犀草素、槲皮素含量,并采用t检验对结果进行比较分析,结果见表9。结果显示,两组数据的方差无显著性差异(P>0.05),表明两种方法计算的含量无显著性差异,一测多评法用于槐花颗粒的多成分质量评价研究是可行的。
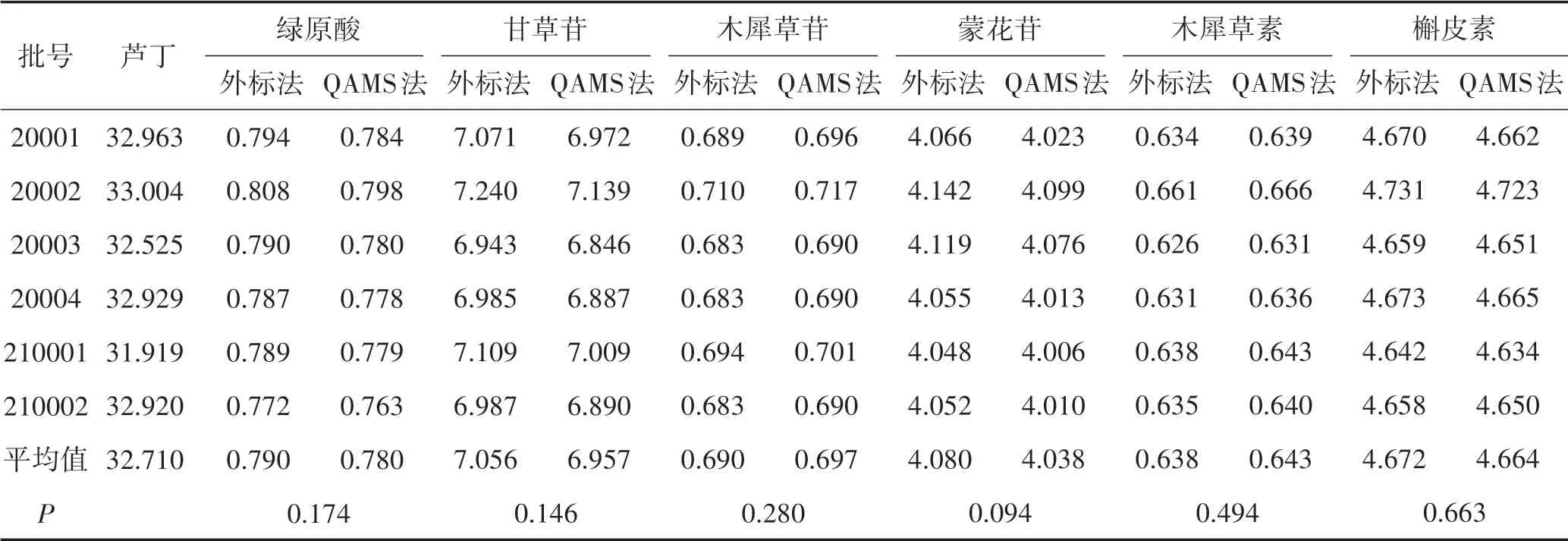
表9 QAMS法与外标法测定结果比较 (mg/g)
3.1 准确度的判断判断QAMS法的准确度,大多是将外标法实测值与QAMS法计算的结果进行t检验后进行评价,如果2种方法测定结果无显著性差异,则说明QAMS法是准确的。如黄帅等[5]在应用QAMS法测定柴胡药材中几种不同皂苷的含量时,采用t检验法来评价QAMS法的准确性和科学性。另外,还可以利用夹角余弦算法来证明QAMS法计算结果与外标法有无显著性差异,陈驰等[6]在应用QAMS法测定人参中不同人参皂苷的含量时就是采用夹角余弦算法来进行验证。t检验法较夹角余弦算法更简单易行,且认可度较高,因此,本文采用t检验法对QAMS法和外标法的测定结果进行精准度的判断。
3.2 内参物的选择研究发现,槐花颗粒中的绿原酸具有抑菌、抗氧化、抗病毒等作用[7];
芦丁具有维生素P样作用和抗菌抗炎等作用[8];
甘草苷具有抗抑郁、保护神经、保肝、抗氧化等作用[9];
木犀草苷具有呼吸系统及心脑血管保护作用、抗肿瘤、抗菌、抗炎、抗病毒等作用[10];
蒙花苷具有抗衰老、抗缺氧和促进凝血等作用[11];
木犀草素具有抗肿瘤、抗菌、抗病毒、消炎、抗过敏等作用[12];
槲皮素具有抗氧化、清除自由基和免疫调节等作用[13]。所以本试验选取上述7种成分为目标化合物,且上述成分含量相对较高,能作为槐花颗粒质量评价的指标。其中芦丁化学性质稳定,在槐花颗粒处方中含量较高,且芦丁易于制备,价格便宜,将其作为内参物时,相对校正因子较稳定,能体现QAMS法操作便捷、成本低以及效率高的特点,故选择芦丁为内参物。
3.3 QAMS法对待测色谱峰定位的重现性考察参考相关文献[14-16],本试验通过考察不同品牌的高效液相色谱仪和色谱柱中各待测成分与芦丁内参物rI/S的重现性。试验结果显示,可通过芦丁与槐花颗粒中另外6种成分的相对保留时间来实现色谱峰定位,且相对保留时间的测定经常用于色谱研究中,重现性可靠,方法简便,可操作性强。
本试验建立的一测多评法适用于槐花颗粒中7种有效成分的含量测定,相对校正因子稳定;
该法不仅节约检测成本、缩短检测时间,而且简化了槐花颗粒的定量检测方法,具有很强的实用性,可为槐花颗粒后续的质量评价提供参考。










