钠盐替代物对全蛋液功能特性的影响
时间:2023-06-08 18:45:14 来源:雅意学习网 本文已影响 人 
佟 平,臧 凤,2,侯裕梁,2,陈红兵,3,高金燕
(1.南昌大学 食品科学与技术国家重点实验室,江西 南昌 330047;
2.南昌大学食品学院,江西 南昌 330047;
3.南昌大学中德联合研究院,江西 南昌 330047)
鸡蛋具有蛋白质含量高、生物利用率高、营养价值高、应用广泛、成本低和可实用性高等优点[1],鸡蛋打蛋去壳后,将蛋液经一定处理后包装,替代鲜蛋消费的产品为液蛋。液蛋能有效解决鲜蛋在运输、贮藏过程中易破碎的问题,更卫生、便捷,且液态蛋有利于集中处理利用蛋残液和蛋壳,并能有效解决沙门氏菌等致病菌隐患,更加符合食品安全性要求[2-3]。同时,液蛋也具有良好的功能特性,如起泡特性、乳化特性和凝胶特性等。起泡特性影响食品结构的膨化程度,蛋液在进行搅打的过程中,蛋白质吸附到起泡表面,降低其表面张力,导致蛋白质变性,进而使泡沫稳定[4]。乳化特性影响产品的味道和内部结构,蛋白质的表面疏水性和溶解度等都会影响液蛋的乳化性能[5]。凝胶特性不仅可以改进食品的形状和质地,还可以提高持水力等,是蛋白质分子聚集形成蛋白质网状的过程,在食品加工生产过程中具有重要作用[6]。因此,具有高功能性的液蛋产品一直是餐饮服务行业和其他商业食品制造商的追求。
液蛋的功能特性在加工过程中受到多种因素影响,通过加热或添加不同种类的添加物可改善液蛋制品的功能特性[7-13]。氯化钠作为最常见的盐之一,可以对蛋白质进行修饰,使盐溶性蛋白溶解,已被广泛用于增强蛋制品的功能特性[14]。Li Junhua等[10]研究了氯化钠对高度稀释的全蛋液理化和凝胶特性,结果表明全蛋液中添加氯化钠可以增加卵白蛋白(ovalbumin,OVA)的表面疏水性,同时还能有效改善全蛋凝胶的结构和质地。Xu Lilan等[15]用氯化钠处理蛋黄液,改变了蛋黄蛋白的空间结构,同时使蛋黄中的可溶性蛋白和游离巯基含量增加。然而,大量研究证实,高膳食钠盐摄入会升高血压,损害心血管系统,并产生其他有害影响[16]。因此,使用氯化钠改善液蛋功能特性可能不是一个很好的选择。
简单地去除或减少氯化钠会对产品质量、可接受性和保质期等产生负面影响[17],这不仅仅是减少氯化钠添加量那么简单,因此,人们将目光转向寻找可以替代氯化钠的其他盐类。已有研究表明,氯化钾和氯化镁能够通过改变蛋白质的结构和聚集程度对蛋白质的功能特性产生积极影响[18]。Wang Xufeng等[19]分析了钙离子和镁离子对大豆分离蛋白乳液凝胶性能的影响,结果表明氯化镁和硫酸镁加入后大豆分离蛋白乳液的凝胶性能显著提高,具有更好的凝胶硬度和弹性。Luo Yu等[20]研究了氯化钾和氯化钠对玉米淀粉-莨菪多糖复合物凝胶特性的影响,结果表明,氯化钾和氯化钠对玉米淀粉-莨菪多糖复合物具有相似的影响,均使玉米淀粉-莨菪多糖复合物的凝胶持水性显著提升。Kim等[21]用氯化镁替代氯化钠,使减脂乳化型猪肉香肠的持水能力和色度得到显著提高,与对照组相比具有更好的质量。齐鹏辉等[22]研究氯化钾部分替代氯化钠对肌原纤维蛋白凝胶性质的影响,结果表明添加0.4 mol/L氯化钠+0.2 mol/L氯化钾的复合盐能显著提高凝胶的持水性和凝胶强度,可以增强对结合水及不易流动水的结合能力。Zhang Dong等[23]用氯化钾替代氯化钠加入咸猪肉中,研究证明氯化钾替代组的咸猪肉水分含量较高,同时还会导致咸猪肉中蛋白质的氧化降解,具有良好的功能特性。在GB 2760—2014《食品添加剂使用标准》中,氯化钠、氯化钾和氯化镁均可用于食品生产中。近年来,氯化钾和氯化镁也逐渐应用于蛋制品方面的研究[24],对蛋制品的相关研发具有重要意义,提示氯化钾和氯化镁或许可以替代氯化钠用于液蛋制品,但它们是否会改变液蛋的理化和功能特性,仍需要进一步探索。
本研究以全蛋液为原料,向其中添加不同浓度的氯化钠、氯化钾和氯化镁,研究这3种氯化盐对全蛋液理化和功能特性的影响,同时对其功能特性的变化进行分析,探究氯化钾、氯化镁替代氯化钠加入液蛋中的可行性。研究结果不仅可拓宽鸡蛋产品市场,显著提升鸡蛋产业附加值,而且可满足人们对安全、健康的功能食品的需求,其潜在的经济价值和市场前景不言而喻。
1.1 材料与试剂
新鲜鸡蛋 市售;
氯化钠、氯化钾和氯化镁(食品级,纯度均大于95%) 河南万邦化工科技有限公司;
其他试剂均为分析纯。
1.2 仪器与设备
恒温磁力搅拌水浴锅 常州迈科诺仪器公司;
RH basic 2磁力搅拌器、S18N-19G高速分散机 德国IKA公司;
Centrifuge 5804 R高速冷冻离心机、Varioskan Lux多功能酶标仪 美国Thermo Scientific公司;
PB-10 pH计德国Sartorius公司;
NS810分光测色仪 深圳三恩时科技有限公司;
TA-XT plus质构分析仪 英国Stable Micro System公司。
1.3 方法
1.3.1 样品制备
新鲜鸡蛋清洗并手工去壳,室温下使用高速分散机以4 000 r/min搅拌30 min,经0.95 mm的筛网去除鸡蛋系带,分别向全蛋液中加入氯化钠、氯化钾和氯化镁,参考GB 2760—2014中氯化钠、氯化钾和氯化镁在乳制品和热凝固蛋制品的添加标准进行浓度设定,氯化钠浓度分别为0.2、0.4、0.8、1.6 mol/L,氯化钾浓度分别为0.2、0.4、0.8、1.6 mol/L,氯化镁浓度分别为5、10、20、40 mmol/L。室温下磁力搅拌至完全溶解后待用。
1.3.2 pH值测定
室温下,将样品置于烧杯中,用pH计测定样品的pH值,3 次平行,取平均值。
1.3.3 色度的测定
用色差仪分别读出样品的色差值,3 次平行取平均值。计算公式如下:

式中:ΔE表示颜色变化的程度;
L*为亮度;
a*正值时表示为偏红,负值时表示为偏绿;
b*正值时表示为偏黄,负值时表示为偏蓝。
1.3.4 表面疏水性测定
参照Li Junsheng等[25]并略作修改。将样品稀释至蛋白质量浓度约为1 mg/mL,取200 μL样品与40 μL浓度为0.005 mol/L 8-苯氨-1-萘磺酸溶液混合,室温下避光反应15 min,设定多功能酶标仪激发波长为350 nm,发射波长为400~700 nm,测定样品荧光强度,用最大荧光强度表征全蛋液的表面疏水性。
1.3.5 蛋白溶解度测定
选用考马斯亮蓝法测定,样品4 ℃、10 000×g离心20 min,用0.001 mol/L pH 7.0磷酸盐缓冲液将上清液稀释至0.1 mg/mL,取20 μL样液与200 μL考马斯亮蓝混合,避光反应10 min,用多功能酶标仪在595 nm波长处测定样品吸光度并计算蛋白质量浓度C1。离心前样品用同样的方法测定蛋白质量浓度C0。溶解度计算公式如下:

1.3.6 起泡特性测定
参照Brückner-Gühmann等[26]并略作修改。样品用0.01 mol/L pH 7.0磷酸盐缓冲液稀释至蛋白质量浓度约为1 mg/mL,取40 mL样液于100 mL量筒内,在高速分散机10 000 r/min条件下搅打30 s,分别在0 min和静置60 min时测定泡沫体积。起泡能力和泡沫稳定性计算公式如下:
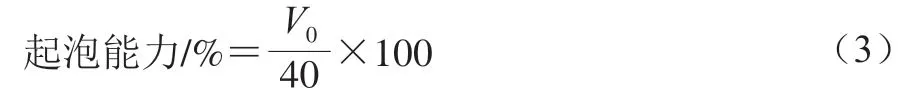
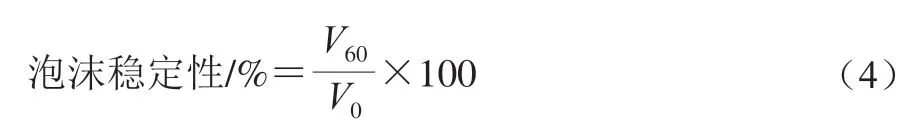
式中:V0为0 min时泡沫体积;
V60为静置60 min后泡沫体积。
1.3.7 乳化特性测定
参照叶凤凌等[27]并略作修改。样品用0.01 mol/L pH 7.0磷酸盐缓冲液稀释至蛋白质量浓度约为1 mg/mL,样品与葵花籽油体积比3∶1混合,在10 000 r/min条件下用高速分散机搅打2 min,分别在0 min和静置10 min取最底层乳化液50 μL加入到5 mL 0.1%的十二烷基硫酸钠(sodium dodecyl sulfate,SDS)溶液中混匀,以0.1% SDS溶液为空白对照,在500 nm波长处测定吸光度。计算公式如下:
式中:A0为0 min样品的吸光度;
A10为10 min样品的吸光度。
1.3.8 凝胶特性测定
1.3.8.1 凝胶持水性
参照Xia Tianlan等[28]方法并略作修改,称取一定质量凝胶样品,4 000 r/min离心10 min,凝胶持水性计算公式如下:
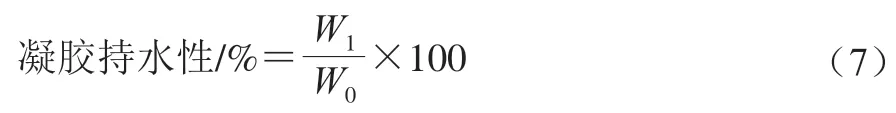
式中:W0为离心前的凝胶质量;
W1为离心后的凝胶质量。
1.3.8.2 质构特性
采用质构仪的TPA模式测定凝胶质构特性,取6 mL样品加入制冰模具中,90 ℃水浴加热30 min,取出后立即置于冰水浴中冷却20 min,4 ℃过夜贮存使凝胶成熟。使用P/50R探头分两次压缩进行测定,测前速率为5.0 mm/s,探头以2.0 mm/s速率穿刺,测后速率为2.0 mm/s,压缩比例50%,触发力为5.0 g,触发类型为Auto,平行3 次测定相关的质构指标。
1.4 数据统计与分析
所有数据利用Microsoft Excel 2010软件进行统计处理,采用GraphPad 8.0软件进行作图分析,用SPSS软件(17.0 版本)对数据进行方差分析,在95%的置信区间用Duncan分析法比较均值。
2.1 钠盐替代物浓度对全蛋液pH值的影响
pH值的变化会导致氨基酸的质子化或非质子化,改变蛋白质分子的表面净电荷,影响蛋白质分子与水分子之间的结合能力,进而影响蛋白质的聚集程度[29]。添加盐的种类和浓度会影响全蛋液的pH值,分别添加氯化钠、氯化钾和氯化镁后,全蛋液的pH值变化见表1。高浓度的氯化钠(0.8 mol/L和1.6 mol/L)显著降低全蛋液的pH值,而分别添加氯化钾和氯化镁后全蛋液的pH值无显著差异。氯化钠具有调节全蛋液中盐类水解、避免引起细胞渗透压的作用,全蛋液中离子强度改变会影响盐类的水解,改变了电离平衡,进而改变了pH值。全蛋液是一个复杂的多蛋白体系,其中大多数蛋白等电点在7.0以下,全蛋液中添加氯化钠后,较低的pH值可能更有利于蛋白质间的静电相互作用,从而影响全蛋液的功能特性[30]。
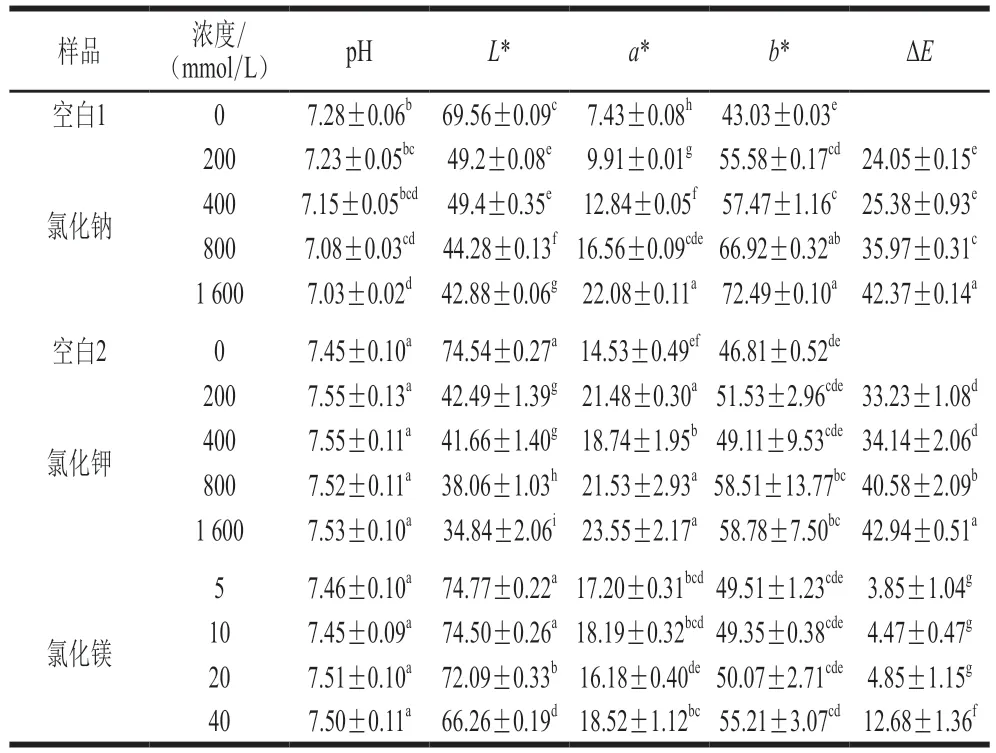
表1 氯化钠、氯化钾和氯化镁浓度对全蛋液pH值和色度的影响Table 1 pH and color of liquid whole egg with different concentrations of sodium chloride, potassium chloride or magnesium chloride
2.2 钠盐替代物浓度对全蛋液色度的影响
全蛋液的颜色是影响消费者对其可接受度的重要因素,消费者通常会将全蛋液的颜色与质量和新鲜度联系在一起,作为评价全蛋液的一个重要指标。全蛋液的颜色主要由蛋黄决定,蛋鸡食用的饲料和技术会影响全蛋液的颜色,但是蛋制品加工同样也会导致其颜色发生变化。本研究中(表1),分别添加氯化钠、氯化钾和氯化镁后,全蛋液的色度呈现出相似趋势,红度和黄度提升而亮度减弱,这可能是由于这3种盐均含有氯离子,这些氯离子会与全蛋液中的类胡萝卜素结合,使发色团吸收峰移动,从而导致全蛋液色度的变化[31]。与添加氯化钠相比,加入氯化镁后全蛋液的颜色变化程度较小,可能是由于氯化镁的添加量较小,不足以使全蛋液的颜色发生较大变化。
2.3 钠盐替代物浓度对全蛋液表面疏水性的影响
表面疏水性通过改变蛋白质的界面性质影响蛋白质的功能特性,由外源性荧光光谱的最大荧光强度表征全蛋液蛋白的表面疏水性[32]。分别添加氯化钠、氯化钾和氯化镁后全蛋液的表面疏水性如图1所示。添加氯化钠后全蛋液的表面疏水性下降(图1A),可能是由于氯化钠的加入掩埋了疏水基团,降低多肽的表面疏水性[33]。Con等[34]也通过实验证明了部分金属盐可以通过疏水相互作用使蛋白质分子聚集在一起,从而降低表面疏水性。而添加氯化钾和氯化镁后全蛋液的表面疏水性呈现出先下降后上升的趋势,在氯化钾和氯化钠添加浓度较低时,全蛋液表面疏水性下降,但随着添加浓度的增大表面疏水性也随着升高。这可能是由于钾离子和镁离子在低浓度时会与蛋白质结合,将表面疏水基团隐藏在内部,而在高浓度时反而会引起排斥蛋白质。

图1 氯化钠(A)、氯化钾(B)和氯化镁(C)浓度对全蛋液表面疏水性的影响Fig. 1 Surface hydrophobicity of liquid whole egg with different concentrations of NaCl (A), KCl (B) or MgCl2 (C)
2.4 钠盐替代物浓度对全蛋液蛋白溶解度的影响
添加氯化钠、氯化钾和氯化镁后,全蛋液蛋白溶解度如图2所示。含氯化钠的全蛋液溶解度表现出先上升后下降的趋势,这可能是因为盐析效应在低浓度下增加了蛋白质的表面电荷并增强了蛋白质和水分子之间的结合,同时,盐析效应屏蔽了分子间的电荷,导致高浓度蛋白质的聚集和沉淀。氯化钾的添加显著提高了全蛋液蛋白的溶解度,其中0.2 mol/L氯化钾改善全蛋液溶解度效果更佳,提高了18.68%。此外,高浓度氯化镁同样会改善全蛋液的溶解度,由图2C可看出,20 mmol/L和40 mmol/L氯化镁添加后,蛋白质的溶解性提高了12.7%和13.8%。3种氯化盐均不会破坏全蛋液的溶解度,反而会显著改善溶解度。当外在因素干扰蛋白质和蛋白质之间的相互作用(例如增加表面电荷)时,蛋白质和水分子之间的作用以及溶解性均会增强,相反则会减弱蛋白质和水分子之间的相互作用,导致溶解性降低[35]。综上所述,添加一定浓度的氯化镁和氯化钾对改善蛋白质溶解度的作用与添加NaCl的效果相似。
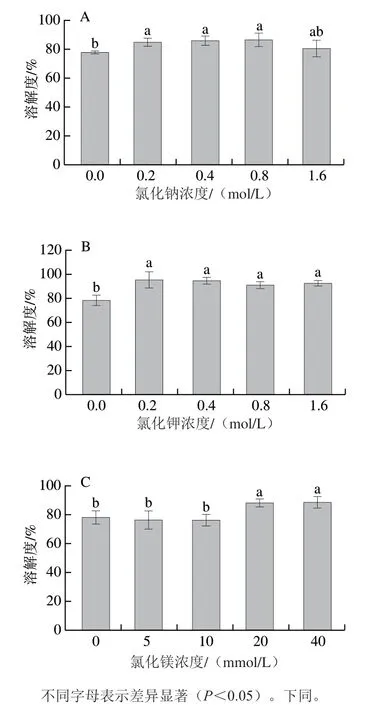
图2 氯化钠(A)、氯化钾(B)和氯化镁(C)浓度对全蛋液蛋白溶解度的影响Fig. 2 Protein solubility of liquid whole egg with different concentrations of NaCl (A), KCl (B) or MgCl2 (C)
2.5 钠盐替代物浓度对全蛋液起泡特性的影响
全蛋液起泡特性取决于蛋清蛋白,蛋清中的OVA、卵类黏蛋白(ovomucoid,OVM)和卵类黏蛋白-溶菌酶(lysozyme,LYS)的复合物均对全蛋液的起泡特性起着关键作用,其中OVA可提高全蛋液的起泡能力,OVM和OVM-LYS的复合物可提高全蛋液的泡沫稳定性[36]。而起泡能力和泡沫稳定性是评价起泡特性的两个重要参数。如图3所示,氯化钠不会导致全蛋液的泡沫稳定性发生显著变化,但是0.2 mol/L和1.6 mol/L的氯化钠会使全蛋液的起泡能力得到显著提升。氯化钾对全蛋液的起泡能力无显著影响,但是添加0.8 mol/L和1.6 mol/L氯化钾后,全蛋液的泡沫稳定性分别提高了21.4%和21.6%,原因可能是较低和较高浓度的氯化钾加入后造成全蛋液表面疏水性增加,更高的表面疏水性有利于降低蛋白质吸附到气-液界面的动力学势垒[37]。氯化镁也不会导致全蛋液的泡沫稳定性发生显著变化,但是20 mmol/L的氯化镁加入后,全蛋液的起泡能力显著降低,这可能归因于较高的溶解度和离子强度[38]。由以上可说明不同金属离子对全蛋液起泡特性的影响存在差异。
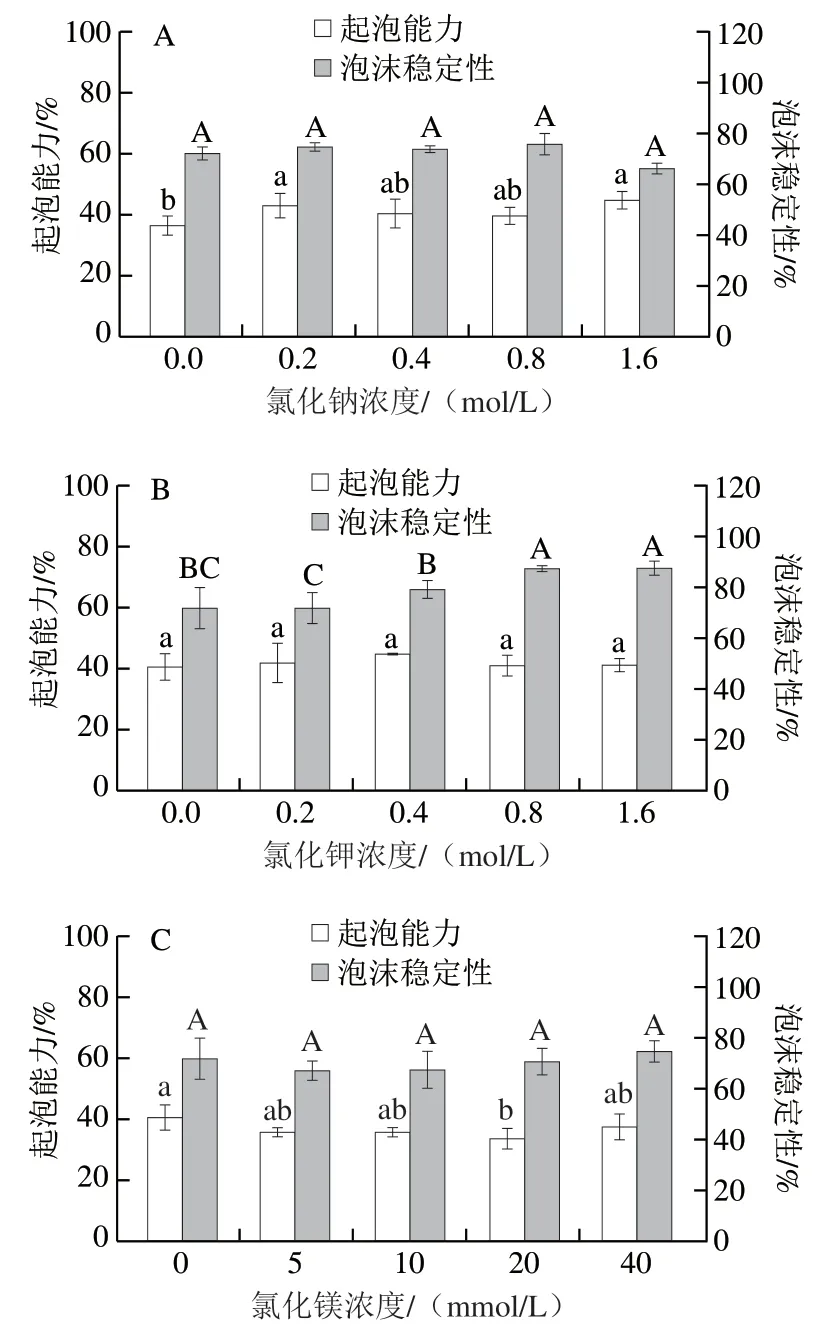
图3 氯化钠(A)、氯化钾(B)和氯化镁(C)浓度对全蛋液起泡特性的影响Fig. 3 Foaming capacity and foam stability of liquid whole egg with different concentrations of NaCl (A), KCl (B) or MgCl2 (C)
2.6 钠盐替代物浓度对全蛋液乳化特性的影响
鸡蛋的乳化特性主要是由蛋黄决定,但完整的鸡蛋也被认为是一种良好的乳化剂。鸡蛋中的蛋白是一种天然的乳化剂和稳定剂,因为它具有两亲性,可以将疏水基团和亲水基团分别向油相和水相重组[39]。由图4可看出,添加0.2 mol/L和0.8 mol/L的氯化钠均会使全蛋液的乳化能力显著降低,而添加1.6 mol/L的氯化钠后全蛋液的乳化能力明显增强。添加氯化钾浓度为0.2 mol/L和0.4 mol/L时,全蛋液的乳化能力与不添加盐时全蛋液的乳化能力相比无显著差异,而氯化钾浓度为1.6 mol/L时,全蛋液的乳化能力明显增强。添加氯化钾后得到与添加氯化钠相似的效果,原因可能是当氯化钠和氯化钾的浓度较低时,离子强度的增加有利于油滴的聚集,导致乳液分层不稳定,同时乳滴之间的斥力随之增强从而导致乳滴之间的凝聚力降低,而随着浓度的增大,静电屏蔽作用使乳滴之间的斥力减弱,进而使全蛋液的乳化能力增高[40]。此外,添加氯化镁后,全蛋液的乳化能力均显著性增强,同时,高浓度的氯化镁也会增强全蛋液的乳化稳定性,添加20 mmol/L和40 mmol/L的氯化镁后,全蛋液乳化稳定性分别提高了14.7%和24.1%,其原因可能是因为Mg2+能够打开蛋白质的空间结构,从而改变蛋白质表面的亲水/亲油性,使蛋白质在油/水界面上的吸附能力增强[19,41]。综上,全蛋液中添加高浓度氯化镁(20 mmol/L和40 mmol/L)对改善全蛋液乳化特性的效果强于氯化钠和氯化钾,可替代氯化钠加入到全蛋液中。

图4 氯化钠(A)、氯化钾(B)和氯化镁(C)浓度对全蛋液乳化特性的影响Fig. 4 Emulsifying capacity and emulsion stability of liquid whole egg with different concentrations of NaCl (A), KCl (B) or MgCl2 (C)
2.7 钠盐替代物浓度对全蛋液凝胶持水特性的影响
水分保持或水结合是蛋白质的重要功能之一,通常称蛋白质凝胶的这种特性为持水能力,导致全蛋液凝胶特性发生改变的蛋白是OVM[42]。全蛋液的持水能力会影响质构和产量,持水能力较好时全蛋液在运输、贮藏过程中其质量几乎不会受到损失,具有良好的品质[43]。
添加氯化钠、氯化钾和氯化镁后,全蛋液的凝胶持水性见表2。添加氯化钠后,全蛋液的凝胶持水性无显著性变化。低浓度的氯化钾(0.2、0.4 mol/L和0.8 mol/L)会显著降低全蛋液的凝胶持水性,其中添加0.2 mol/L氯化钾后全蛋液的凝胶持水性降低最显著,而添加氯化钾1.6 mol/L时,与空白组相比无显著差异,这可能是由于低浓度的钾离子增强了蛋白质的表面张力,使蛋白质结构更加松弛,从而使持水性下降[23]。同时,低浓度的氯化镁(5 mmol/L)使全蛋液的凝胶持水性显著降低,而较高浓度的氯化镁(10、20 mmol/L和40 mmol/L)与空白组相比又无显著差异,可能是蛋白分子分散,形成网状结构时不紧密导致。故1.6 mol/L氯化钾和较高浓度的氯化镁(10、20 mmol/L和40 mmol/L)均可替代氯化钠加入到全蛋液中。
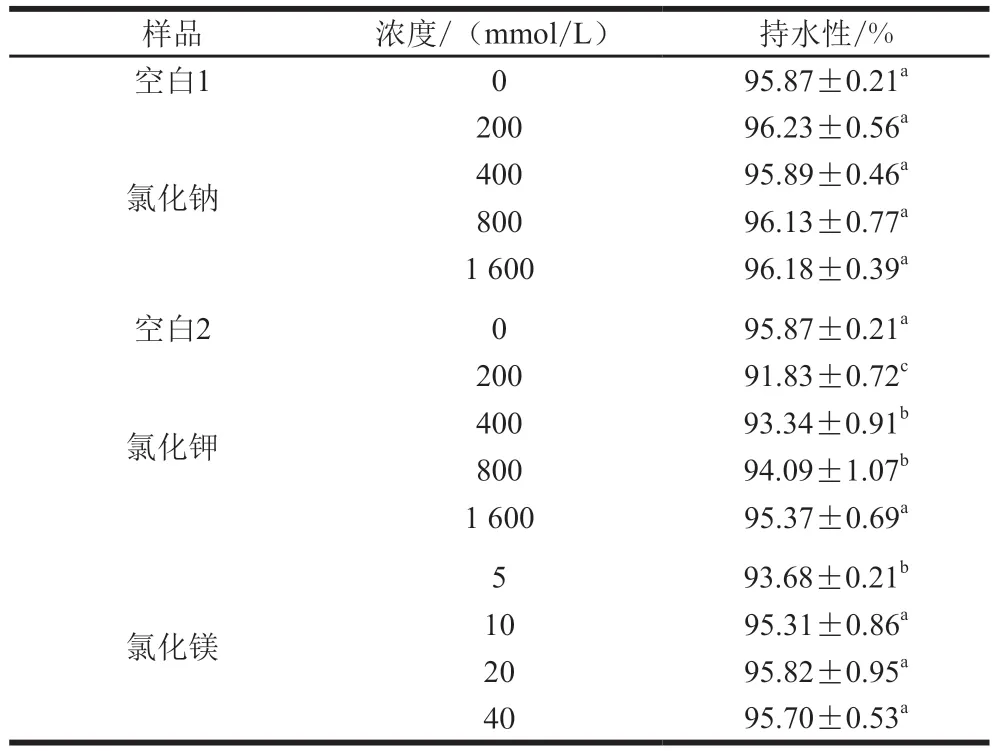
表2 氯化钠、氯化钾和氯化镁浓度对全蛋液持水特性的影响Table 2 Water-holding capacity of liquid whole egg gels with different concentrations of sodium chloride, potassium chloride or magnesium chloride
2.8 钠盐替代物浓度对全蛋液凝胶质构特性的影响
硬度和弹性是凝胶质构特性的两个重要参数,添加氯化钠、氯化钾和氯化镁后全蛋液的凝胶质构见表3。全蛋液硬度随着氯化钠浓度的升高呈先升高后降低的趋势,这可能是因为低浓度的氯化钠增加了全蛋液的溶解度,使更多的卵黄高磷蛋白和高密度脂蛋白分散在凝胶三维网络中,增加了全蛋液的凝胶硬度[44],而高浓度氯化钠可能会屏蔽蛋白质之间的静电力,使全蛋液的硬度降低。分别添加氯化钾和氯化镁后全蛋液的凝胶硬度具有相似的趋势,即先降低后升高。添加0.2 mol/L氯化钾和5 mmol/L氯化镁后,全蛋液凝胶硬度均显著下降,这与全蛋液的表面疏水性变化一致,低浓度时,钾离子和镁离子与蛋白质结合,将表面疏水基团隐藏在内部使表面疏水性降低。而随着盐浓度的增大凝胶硬度也表现出上升的趋势,添加40 mmol/L氯化镁后,凝胶硬度超过空白组的凝胶硬度,这可能是因为Mg2+有助于形成致密的蛋白质聚集体并促进凝胶均匀性和抗变形性[45]。随着氯化钠浓度的升高,弹性逐渐降低,而氯化钾和氯化镁的加入弹性无明显变化。综上,1.6 mol/L的氯化钾和40 mmol/L的氯化镁均可替代氯化钠改善全蛋液的凝胶质构特性。
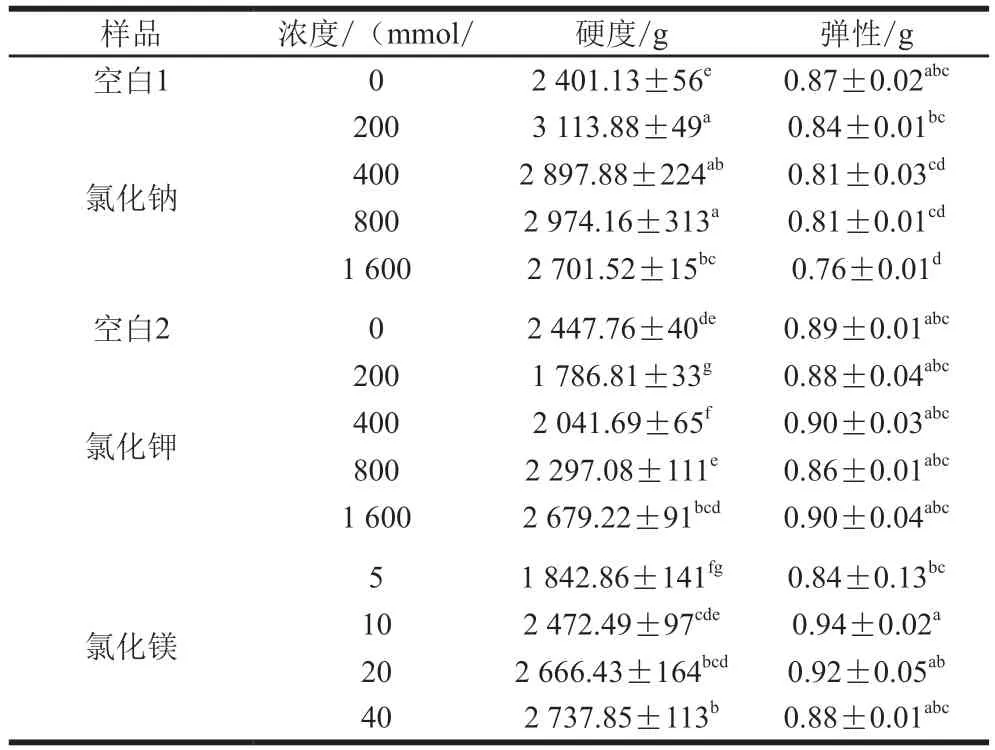
表3 氯化钠、氯化钾和氯化镁浓度对全蛋液质构特性的影响Table 3 Textural properties of liquid whole egg gels with different concentrations of sodium chloride, potassium chloride or magnesium chloride
比较氯化钠、氯化钾和氯化镁对全蛋液理化性质和功能特性的影响。总体而言,氯化钠的加入改善了全蛋液的溶解性、起泡性和凝胶硬度,而乳化性明显降低。与添加氯化钠相比,较高浓度的氯化镁(20 mmol/L和40 mmol/L)添加后全蛋液的乳化能力和乳化稳定性均显著提高,同时蛋白质的溶解性也得到了显著改善。此外,添加40 mmol/L的氯化镁后,全蛋液的持水性和弹性均未被破坏,凝胶硬度显著增高,在全蛋液的凝胶能力方面优于氯化钠,同时全蛋液的颜色变化程度较低且不会引起全蛋液的pH值出现显著变化。综合来看,全蛋液中添加40 mmol/L氯化镁最具有替代氯化钠的潜力。本研究中氯化钠、氯化钾和氯化镁的添加量严格依据GB 2760—2014设置,考虑到3种盐的最大使用量不同,所以在此研究中3种盐并没有设置相同的添加浓度。另外,在实际的工业生产中,氯化钾和氯化镁一般不是单一作为钠盐替代物使用,不同盐混合添加效果可能更佳,所以为扩大钠盐替代物在液蛋制品中的应用,还需更多的研究确定钠盐替代物的最佳混合比例。
猜你喜欢 氯化镁氯化钾蛋液 约旦APC与印度IPL签署氯化钾合同中国化肥信息(2022年6期)2023-01-06东方铁塔:氯化钾产品供应紧张中国化肥信息(2022年3期)2023-01-05海绵钛倒U型反应器中排氯化镁管固定结构优化钛工业进展(2022年4期)2022-09-15黑枣醋蛋液理化特性、挥发性物质变化及抗氧化能力比较分析食品工业科技(2022年12期)2022-06-11氯化钾镀锌层发雾故障原因表面工程与再制造(2022年1期)2022-05-25无水氯化镁中低含量碱式氯化镁测定研究盐科学与化工(2022年5期)2022-05-19黄瓜“厚蛋烧”食品与健康(2020年7期)2020-07-09药用氯化镁生产过程中水分控制分析天津化工(2020年2期)2020-05-09氯化钾2018年上行明显2019年涨势或将放缓中国化肥信息(2019年2期)2019-04-04千层厚蛋烧饮食科学(2017年7期)2017-09-03









