广西地不容非药用部位化学成分研究
时间:2023-06-24 08:35:03 来源:雅意学习网 本文已影响 人 
张汝胜, 李 霞, 黄永林, 王亚凤, 阳丙媛, 李典鹏, 何瑞杰*
( 1. 桂林理工大学 化学与生物工程学院, 广西 桂林 541006;
2. 广西植物功能物质与资源持续利用重点实验室,广西壮族自治区中国科学院 广西植物研究所, 广西 桂林 541006 )
广西地不容(Stephaniakwangsiensis)属于防己科(Menispermaceae)千金藤属(Stephania)多年生草质落叶藤本植物,长超过3 m,块根通常扁球形,叶互生、纸质,叶柄于叶基部1~1.5 cm处盾状着生、长4~9 cm,叶片三角状圆形至近圆形,主产于我国广西西北部至西南部,生于石灰岩地区的山地灌丛(中国科学院中国植物志委员会,1996)。防己科植物大多含有丰富的生物碱,具有较高的药用价值。广西地不容药用部位(块根)含有丰富的生物碱,具有很好的生物活性,如镇痛和抗炎作用(罗昱澜等,2017)、抑菌活性(邓业成等,2006)、杀虫活性(邓业成和徐汉虹,2005)、抗病毒活性(郝静等,2008)。在临床上主要用于镇痛、解热(王宪楷和赵同芳,1990)、镇静(金国章,1987)等。广西地不容作为广西地方特色药用植物,其非药用部位(茎、叶)的资源存量巨大,而对于野生资源日益匮乏的今天,从非药用部位中寻找可替代药用部位中一些有效成分的研究显得尤其重要。
广西地不容植物富含生物碱,由于该类成分在分离纯化过程中极易被柱材料吸附,从而导致拖尾严重、收率低,因此生物碱的分离一直是天然产物研究领域的一个热点和难点问题。本研究以广西地不容非药用部位(茎、叶)为对象,依托现代先进的仪器设备,采用Sephadex LH-20、碱化硅胶、聚酰胺、MCI gel CHP-20P等多种柱色谱法和现代波谱学技术以及现代药理学技术,拟探讨以下问题:(1)广西地不容非药用部位甲醇提取物中的化学成分;
(2)所分离得到的部分化合物的抗菌活性。
1.1 材料、仪器和试剂
植物材料:广西地不容地上部分于2019年8月采自广西桂林恭城瑶族自治县,经广西植物研究所黄俞淞副研究员鉴定为广西地不容(Stephaniakwangsiensis)的非药用部位,标本(编号:20190824)保存于广西植物功能物质与资源持续利用重点实验室。
供试菌种:所用菌种为大肠杆菌(Escherichiacoli)、金色葡萄球菌(Staphylococcusaureus)、枯草芽孢杆菌(Bacillussubtilis)、尖孢镰刀菌(Fusariumoxysporum),均由桂林理工大学化学与生物工程学院李海云老师课题组提供。
仪器:LC-MS/IF-TOF液质联用色谱仪(日本,岛津公司)、Brucker Avance Ш HD-500 MHz超导核磁共振波谱仪(瑞士,Brucker公司)、OSB-2100油浴锅、真空泵(上海爱朗仪器有限公司)、HH·BII·360-S-II恒温培养箱 (上海跃进医疗器械厂)、SW-CJ-1F超净工作台(苏净集团安泰公司)、TQZ-312振荡器(上海精宏实验设备有限公司)、YXQ-LS-50SII高压灭菌锅(上海博迅实业有限公司医疗设备厂)。
材料与试剂:Sephadex LH-20(GE Healthcare Bio-Science AB,Sweden)、MCI gel CHP-20P(75 ~ 150 μm;
Mitsubishi Chemical, Tokyo, 日本)、硅胶(200 ~ 300目,青岛海洋化工有限公司)、聚酰胺(100 ~ 200目,江苏长丰化工有限公司)、TLC薄层色谱板(德国Merck公司)、LB营养琼脂(青岛高科技工业园海博生物技术有限公司)、LB肉汤(青岛高科技工业园海博生物技术有限公司)、氨苄青霉素(上海源叶生物科技有限公司)、99%生物技术级二甲基亚砜(DMSO,上海麦克林生化科技有限公司)、提取与分离所使用的试剂皆为实验室常用分析纯。
1.2 提取和分离
取干燥广西地不容地上部分4.2 kg,粉碎后用甲醇室温浸提3次,每次30 L,每次1周,合并过滤提取液,减压浓缩后得到浸膏480.1 g。浸膏加蒸馏水使其混悬后依次使用石油醚、乙酸乙酯、正丁醇各萃取3次,减压回收萃取溶剂,得石油醚萃取物44.0 g、乙酸乙酯萃取物33.4 g、正丁醇萃取物80.0 g。取正丁醇萃取物75.0 g上MCI柱层析(7 cm × 80 cm),用甲醇-水(0%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%)进行梯度洗脱,经TLC薄层层析检测后合并得到12个馏分,即Fr.1~Fr.12。将Fr.1(26.3 g)进行Sephadex LH-20柱色谱(甲醇-水,0% ~ 100%,每20%为1个梯度)分离纯化,得到5个馏分,即Fr.1-1~Fr.1-5。将Fr.1-1(16.8 g)进行反复Sephadex LH-20柱层析(20%甲醇-水)得到化合物4(8.7 g)。将Fr.2 (3.6 g)用二氯甲烷∶甲醇∶水体系(36∶1∶0.1,18∶1∶0.1,9∶1∶0.1,V/V/V)进行硅胶柱层析,得到6个馏分,即Fr.2-1~Fr.2-6。将Fr.2-2(1.2 g)用二氯甲烷∶甲醇体系(100∶0~50∶50,V/V)进行聚酰胺柱层析,得到9个馏分,即Fr.2-2-1~Fr.2-2-9。将Fr.2-2-1(0.2 g)用二氯甲烷∶甲醇(1∶1,V/V)进行Sephadex LH-20柱色谱分离纯化得到化合物1(12.0 mg)、2(3.0 mg)、3(6.1 mg)、8(5.3 mg)。将Fr.3 (8.4 g)用二氯甲烷∶甲醇体系(1∶1,V/V)进行反复Sephadex LH-20柱色谱分离,得到6个馏分,即Fr.3-1~Fr.3-6。将Fr.3-3 (1.5 g )用二氯甲烷∶甲醇∶水体系(18∶1∶0.1,9∶1∶0.1,8∶2∶0.2,V/V/V)进行反复硅胶柱层析等色谱技术分离纯化,最终得到化合物5(4.5 mg)、6(5.1 mg)、7(6.3 mg)、9(11.0 mg)、10(3.3 mg)。化合物1-10的化学结构如图1所示。

图 1 化合物1-10的化学结构Fig. 1 Chemical structures of compounds 1-10



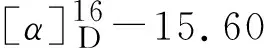
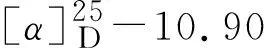
化合物6C20H24NO4,黑色油状。HR-ESI-MSm/z:343.175 8 [M+H]+。1H-NMR (500 MHz, MeOD)δ:6.78 (1H, d,J= 7.9 Hz, H-9), 6.66 (1H, d,J= 7.9 Hz, H-8), 6.37 (1H,s, H-3), 4.09 (1H, d,J= 13.8 Hz, H-15), 3.60 (3H, s, 10-OCH3), 3.53 (1H, br d,J= 12.4 Hz, H-1), 3.71 (3H, s, 2-OCH3), 3.35 (3H, s, N-CH3), 2.90 (3H, s, N-CH3), 2.72 (1H, m, H-4), 2.60 (2H, br t,J= 12.9 Hz, H-7)。13C-NMR (125 MHz, MeOD)δ:148.0 (C-1), 152.4 (C-2), 122.5 (C-3a), 110.1 (C-3), 24.7 (C-4), 62.4 (C-5), 126.3 (C-7a), 31.7 (C-7), 118.4 (C-8), 111.2 (C-9), 151.2 (C-10), 147.6 (C-11), 122.8 (C-12), 118.0 (C-13), 121.3 (C-14), 71.0 (C-15), 56.5 (-OCH3), 54.0 (N-CH3), 56.3 (-OCH3), 43.6 (N-CH3)。以上数据与文献(李海滨,2006;
王建忠等,2013)报道一致,故鉴定化合物6为magnoflorine。

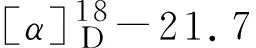
化合物9C20H23NO4,黑色油状。HR-ESI-MSm/z:342.168 5 [M+H]+。1H-NMR (500 MHz, MeOD)δ:7.15 (1H, d,J= 8.2 Hz, H-9), 7.02 (1H, d,J= 8.2 Hz, H-8), 6.81 (1H, s, H-3), 2.58 (3H, s, H-17), 3.68 (3H, s, 2-OCH3), 3.91 (3H, s, 10-OCH3), 3.86 (3H, s, 11-OCH3)。13C-NMR (125 MHz, MeOD)δ:143.2 (C-1), 150.5 (C-2), 113.5 (C-3), 29.28 (C-4), 62.3 (C-5), 64.3 (C-6), 35.9 (C-7), 125.6 (C-8), 112.8 (C-9), 153.5 (C-10),145.5 (C-11), 127.0 (C-12), 119.3 (C-13), 120.6 (C-14), 131.2 (C-15), 128.8 (C-16), 43.9(C-17), 53.8 (2-OCH3), 56.3 (11-OCH3), 56.6 (10-OCH3)。以上数据与文献(邓业成和徐汉虹,2004)报道一致,故鉴定化合物9为紫堇定碱。
化合物10C20H19NO4,黄色针晶。HR-ESI-MSm/z:338.137 2 [M+H]+。1H-NMR (500 MHz, MeOD)δ:7.99 (1H, d,J= 8.6 Hz, H-11), 7.06 (1H, d,J= 8.6 Hz, H-10), 6.71 (1H, s, H-3), 6.25 (1H, d,J= 1.5 Hz, -OCH2O-), 6.10 (1H, d,J= 1.5 Hz, -OCH2O-), 4.09 (3H, s, 8-OCH3), 4.00 (3H, s, 9-OCH3), 2.77 (3H, s, N-CH3)。13C-NMR (125 MHz, MeOD)δ:142.2 (C-1), 123.2 (C-1a), 146.7 (C-2), 107.0 (C-3), 126.7 (C-3a), 29.35 (C-4), 53.8 (C-5), 44.2 (C-6), 62.0 (C-6a), 27.0 (C-7), 116.7 (C-7a), 152.2 (C-8), 146.0 (C-9), 110.4 (C-10), 124.8 (C-11), 130 (C-11a), 100.7 (-OCH2O-), 55.9 (8-OCH3), 60.8 (9-OCH3)。以上数据与文献(彭树林等,1992)报道一致,故鉴定化合物10为克班宁。
3.1 培养基配置
固体培养基的配置:称取LB营养琼脂8 g使其完全溶解于200 mL蒸馏水中,于121 ℃高温下灭菌20 min,备用。
液体培养基的配置:称取LB肉汤5 g 于200 mL蒸馏水中使其完全溶解,于121 ℃高温下灭菌20 min,备用。
3.2 体外抗菌实验
采用滤纸片法测定其抑菌圈的大小。以DMSO为溶剂,准确称取各个化合物,将其配置成6 mg·mL-1的样品溶液,测定各个化合物对各种菌的抑制效果。参照胡野(2004)的方法,具体的实验步骤如下:(1)将实验所用到的滤纸片、镊子、培养皿、三角刮刀、移液枪头等用品用干净的报纸包好后放入高温灭菌锅中,在121 ℃下高温杀菌20 min,备用;
(2)菌种接种,将指示菌种采用划线法接种于制备好的琼脂斜面培养基上,在(36±1)℃的培养箱里培养24 h后放入冰箱内保存,备用;
(3)菌悬液的配制,在相应的琼脂斜面培养基上用接种环在培养好的菌种内取1环菌种放入对应的液体培养基中,在(37±1)℃下进行恒温震荡24 h后,取100 μL培养好的菌悬液,用无菌水稀释300倍,使菌悬液稀释到106~108CFU·mL-1,并置于4 ℃下冷藏,备用;
(4)样品溶液的配置,将准备好的0.6 cm大小的滤纸片经过高温灭菌后,浸泡在配好浓度的样品溶液以及空白对照溶液中1 h左右;
(5)抑菌圈的测定,在无菌操作台中用移液枪吸取200 μL菌悬液于平板固体培养基上,先使用三角刮刀在培养基上均匀涂抹,再放在直径为0.6 cm完全浸满样品的滤纸片上,在(36±1)℃下培养24 h,最后测定其抑菌圈直径。实验平行3次,用DMSO作为阴性对照,用氨苄青霉素(AMP,100 mg·mL-1,即称取100 mg氨苄青霉素溶解于1 mL 1 mol·L-1HCl中)作为阳性对照。
3.3 结果和分析
分别用大肠杆菌、金色葡萄球菌、枯草芽孢杆菌、尖孢镰刀菌作为供试菌,将从广西地不容非药用部位中分离得到的化合物通过滤纸片法测定其抑菌圈的直径,测定结果如表1所示。表1结果显示,与阳性对照AMP比较,化合物1、2、5对大肠杆菌的抑制作用显著降低(P<0.05),化合物2对金色葡萄球菌的抑制率极显著低于阳性对照AMP的抑制率(P<0.01),化合物3和化合物8对枯草芽孢杆菌有弱的抑制作用,但无显著性差异(P>0.05)。
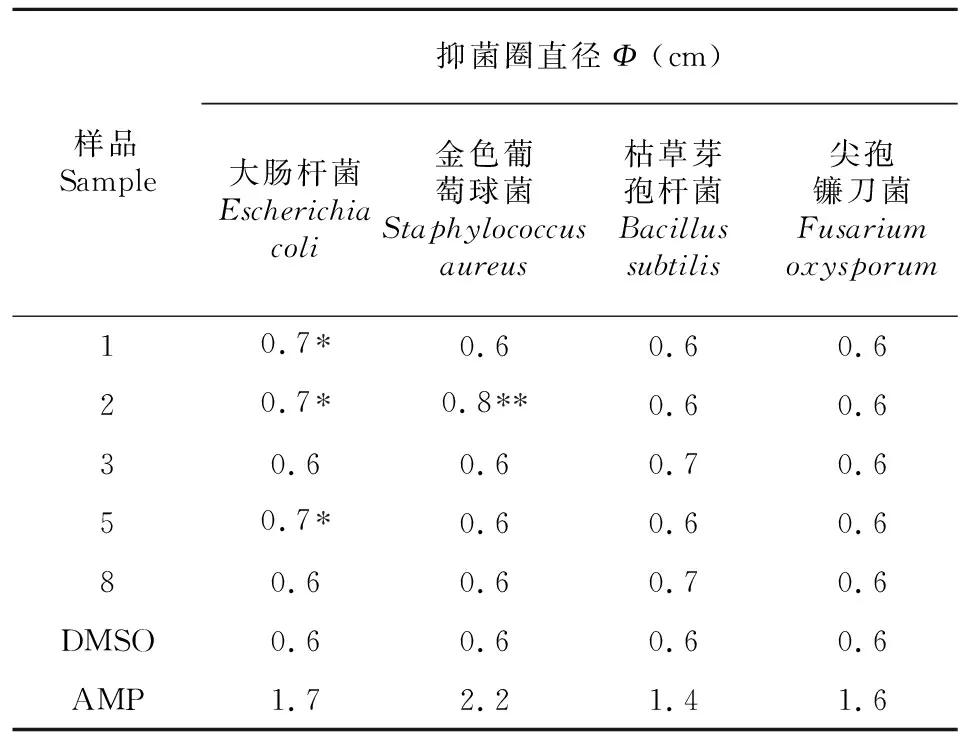
表 1 广西地不容非药用部位化学成分的抑菌活性Table 1 Antimicrobial activities of chemical constituents from non-medicinal parts of Stephania kwangsiensis
本研究从广西地不容非药用部位醇提物中分离鉴定出4个阿朴啡生物碱。其中,异紫堇定碱(3)是“解痉宁”的主要成分,并具有很好的止泻功效,这与沈雅琴和张明发(1998)的研究结果一致, 在临床上主要用于治疗胃肠、 胆、 血管等痉挛所致的疼痛;
Magnoflorine(6)具有使心血管系统处于高动力状态的效用,有利于运动员较长时间维持高强度运动能力,有抗疲劳功效,这与吕莹等(2001)的研究结果一致;
克班宁(10)具有抗心律失常的作用,这与淤泽溥等(1992)的研究结果一致,可诱导人类癌细胞的G1阻滞和凋亡作用(Wongsirisirt et al., 2012),以及通过抑制MAPKs和Akt信号通路表现出抗炎活性(Intayoung et al., 2016)。邓业成等(2006)研究发现,广西地不容药用部位(块根)的提取物具有广谱抗菌作用,而由于本研究从广西地不容非药用部位中所分离得到的化合物在浓度为6 mg·mL-1时对实验所选用的菌种均显示较弱的抑制作用,因此对于非药用部位是否存在较强的抗菌成分还有待进一步研究。广西地不容植物富含生物碱,使用普通柱层析分离会因不可逆吸附产生而导致样品损失量大,本研究使用了氨蒸汽碱化硅胶柱材料,极大地改善了不可逆吸附的产生,提高了分离效率,这与刘吉华等(2013)的研究结果一致。本研究结果为广西地不容植物其他部位以及其他生物碱的分离提供了方法指导。同时,广西地不容的非药用部位(茎、叶)作为中药“金不换”的一个副产物,由于其蕴含多种生物碱成分,如异紫堇定碱、magnoflorine、克班宁已在临床中被广泛使用,因此该部分资源开发潜力巨大,随着更多化学成分被发现以及其药理研究的深入,该部位有作为新药源的可能。










