Mo2C/ZnIn2S4复合材料的制备及其光催化产氢性能研究
时间:2023-01-18 15:30:07 来源:雅意学习网 本文已影响 人 
刘 超 ,谢潇琪 ,范鹏凯 ,李 艳,2
(1.河北地质大学 宝石与材料学院, 河北 石家庄 050031;
2.河北地质大学 硅酸盐固废资源化利用河北省工程研究中心, 河北 石家庄 050031)
目前,人类主要能源仍然依赖于有限的、不可再生的化石燃料。但是化石燃料的过度使用引发了严重的能源危机和环境问题[1]。因此,开发可再生、清洁、环境友好的能源势在必行。太阳能作为一种可持续、清洁的能源正引起人们的极大关注,但在实际应用中,需要将太阳能转换为其他形式的能源,如化学燃料,以便更有效地存储和运输[2-4]。氢能(H2)被认为是一种理想的化学燃料,这主要是因为H2相对于其他化石燃料具有清洁、无毒、能量密度高的优点[5]。太阳能光催化分解水制氢被认为是一种具有广阔前景的太阳能转化为氢能的方法。其中,光催化剂的设计与合成是能量能否高效转化的关键所在,在众多光解水制氢催化剂中,金属硫化物基半导体由于其良好的化学稳定性,合成方法简单,太阳光利用率高等优点而受到了广泛的关注[6]。
金属硫化物由于合适的导带(CB)位置,带隙较窄,具有较好的化学稳定性等被认为是对可见光响应的优良的光催化材料[7-9]。近年来,三元金属硫化物由于具有多种金属元素的性质,逐渐出现在光催化材料的研究中。其中,硫化铟锌(ZnIn2S4,ZIS)由于其光学特性和相对狭窄的可见光响应带隙,成为光解水催化领域研究的热点[10-12]。然而对于单一组分ZIS来说,仍然存在光生电荷分离效率低和电子传输能力差等问题,导致ZIS的光催化活性较差[13]。通过助催化剂的表面修饰可有效促进光生电荷的分离,降低析氢过电势,从而有效提高光催化析氢效率。传统的贵金属助催化剂(例如铂)可显著提高材料光催化析氢效率。但是,贵金属储量稀少且价格昂贵,明显限制了其工业化应用。研究和开发含储量丰富,成本低廉,高效稳定的非贵金属助催化剂具有重要的意义。
研究表明,过渡金属碳化物是一种高效、低成本的贵金属替代催化剂,可作为光催化分解水产氢的助催化剂[14]。碳化钼(MoxC)催化剂作为过渡金属碳化物的重要组成部分,MoxC具有与贵金属相似的d带电子结构,表现出类铂的金属特性,被认为是一种非常有潜力的替代贵金属析氢助催化材料[15-17],近年来受到了广泛关注。此外,MoxC具有成本低、原料丰富、易于制造等优点,具有广阔的应用前景。
本研究以钼酸铵和二氰二胺为前驱体,通过高温固相法制备了Mo2C助催化剂。然后以硝酸锌、硝酸铟和硫代乙酰胺为原料,通过原位生长法制备了Mo2C/ZnIn2S4复合光催化材料,对复合材料的光催化析氢活性进行评价。结果表明,与Mo2C或ZnIn2S4单一组分相比,制备的Mo2C/ZnIn2S4复合材料可见光催化分解水析氢性能显著提高,探讨并提出了Mo2C/ZnIn2S4复合材料光催化析氢反应机理。
1.1 Mo2C及Mo2C/ZnIn2S4材料的制备
称取5g二氰二胺(C2H4N4,AR)加入到40 mL去离子水中,加热搅拌至完全溶解,然后加入2.5 g钼酸铵((NH4)6Mo7O24·4H2O,AR),搅拌溶解,在烘箱中100 ℃干燥,收集白色块状产物并研磨至粉末状前驱体。得到的前驱体氩气气氛保护下在管式炉中以5 ℃/min升温至400 ℃保持30 min,然后以5 ℃/min升温至800 ℃保持6 h,自然冷却到室温。所得到的黑色产物为Mo2C,记为MC。
称取0.03 g上述Mo2C样品超声分散于25 mL去离子水中,得到Mo2C悬浮液。在悬浮液中依次加入0.214 g的硝酸锌(Zn(NO3)2·6H2O,AR),0.433 g硝酸铟(In(NO3)·xH2O,AR),0.435 g硫代乙酰胺(C2H5NS,AR)搅拌至完全溶解。将上述液体转移至高压反应釜升温至160 ℃,保温12 h,自然冷却至室温。将所得产物抽滤,并用水和乙醇清洗数次,60 ℃下干燥过夜。所得复合光催化材料分别标记为10%MC/ZIS(其中,10%代表MC的质量分数)。通过改变Mo2C的加入量得到不同MC负载量对样品,分别记为5%MC/ZIS、20%MC/ZIS和30%MC/ZIS。此外,纯ZnIn2S4采用相同的方法制成,其中,Mo2C加入量为0 g,记为ZIS。
1.2 样品的表征
采用X射线衍射仪(XRD)(德国,Bruker D8 Focus)测定样品的物相结构,使用扫描电子显微镜(SEM)(日本,JEOLJSM-7610F Plus)观察样品的微观形貌,使用荧光分光光度计(日本,日立F-7500)对样品进行光致发光(PL)光谱分析,使用紫外-可见漫反射仪(美国,Thermo Fisher Evolution 220)测试样品紫外-可见漫反射光谱(UV-vis DRS),使用扫描开尔文探针(英国,Kelvin Probe Technology SKP5050)测定材料的表面功函(金作为参比样品),X射线光电子能谱(XPS)测量使用X射线光电子能谱仪(美国,Thermo Fisher ESCALAB 250)测试。等离子体发射光谱仪(ICP,美国,Thermo Fisher iCAP6300)测定复合样品中金属原子的含量。
1.3 光电性能测试
采用三电极体系,Ag/AgCl为参比电极;
以Au为参比,在上海辰华CHI760E电化学工作站上测试了光催化材料的电化学阻抗谱(ESI)和瞬态光电流响应。在电化学测量中,采用标准三电极电池,电解液为Na2SO4(0.2 moL/L)。铂片作为对电极,Ag/AgCl(在饱和KCl中)作为参比电极。工作电极制作过程为:将8 mg粉末样品分散在含有480 μL去离子水、480 μL无水乙醇和40 μL 5% Nafion溶液的混合溶液中,超声分散使其成为均匀的浆液。将30 μL浆液滴到面积为1.0 cm2的FTO玻璃电极上。光电流测试采用带400 nm截止片的300 W氙灯(PLS-SXE300D)作为光源。用标准的三电极体系测量了样品的极化曲线。在0.5 moL/L的H2SO4溶液中,以玻碳电极(覆盖0.2 mg/cm2样品)作为工作电极,石墨棒作为对电极,Ag/AgCl作为参比电极。在5 mV/s的扫描速率下测试线性扫描伏安极化曲线。
1.4 产氢性能测试
光催化析氢实验采用封闭循环装置,在石英反应器中进行。将30 mg的光催化剂添加到含27 mL去离子水、3 mL乳酸(C3H6O3,AR)的混合溶液中,使用300 W Xe灯(PLS-SXE300D)和UV截止滤波器(λ> 400 nm)照射混合物,光源为侧光源,通过循环冷凝水控制反应体系的温度在20 ℃。每1 h采集1 mL所生成气体,在气相色谱仪(GC7900)上检测生成的氢气。通过标准曲线法确定氢气的含量。
2.1 Mo2C/ZnIn2S4的表征与分析
2.1.1 XRD分析
图1为Mo2C、ZnIn2S4和不同比例复合的Mo2C/ZnIn2S4的XRD谱图。由图1可知,Mo2C的主要衍 射 峰 位 于2θ为34.43°、37.34°、39.53°、61.75°和74.50°的位置,分别对应Mo2C(JCPDS No.35-0787)的(100)、(002)、(101)(110)以及(112)晶面,其中,002晶面相对于标准卡片向低角度方向偏移,说明002晶面间距有所增大。样品ZnIn2S4的主要衍射峰位于2θ为21.58˚、27.69˚、47.17˚ 和 52.43˚的位置,分别对应于ZnIn2S4(JCPDS No.65-2023)图的(006)-(102)-(110)以及(116)晶面。Mo2C/ZnIn2S4复合材料则表现出较强ZnIn2S4衍射峰,当Mo2C含量较低时,谱图中并未发现Mo2C特征衍射峰。随着复合样品中Mo2C含量的增加,Mo2C特征峰强度逐渐增大,这主要是由于Mo2C含量较少及分散度较高所致。复合材料中ZnIn2S4(102)晶面衍射峰随Mo2C的比例增加有所增强,可能是由于在Mo2C对ZnIn2S4各晶面的诱导生长速率不同及各向异性生长趋势有关[18,19]。
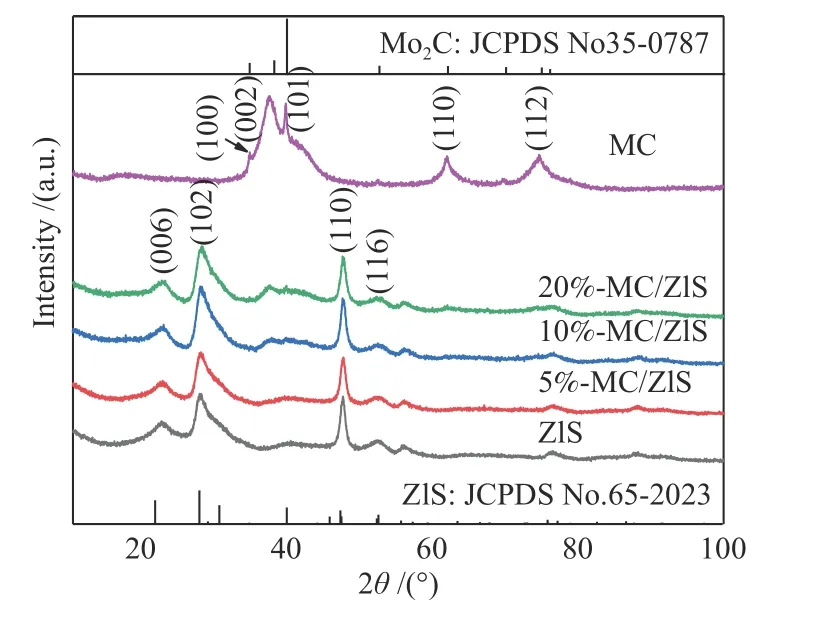
图1 Mo2C,ZnIn2S4和MC/ZIS的XRD谱图Figure 1 XRD patterns of Mo2C, ZnIn2S4 andMC/ZIS composites
2.1.2 SEM分析
用SEM对样品的形态和结构进行了表征,如图2所示。其中,Mo2C表现出不规则的块状形态,并且显示出一定程度的团聚现象,这是高温固相反应易使材料产生团聚的固有缺陷所致。ZnIn2S4表现为薄层状结构,并具有轻微卷曲现象,从而使材料疏松堆积。相对于块体结构,这种结构使材料具有更多的活性位点暴露[20],有利于光催化反应过程中的H+吸附。而Mo2C/ZnIn2S4复合材料中ZnIn2S4均匀的沉积在Mo2C的表面,且保留了原有的层状结构。

图2 Mo2C、ZIS和10%MC/ZIS的SEM照片Figure 2 SEM images of Mo2C (a), ZIS (b) and 10%MC/ZIS (c)
2.1.3 UV-vis DRS分析
材料的光谱相应范围和禁带宽度对光催化剂的催化效率有重要影响,对ZnIn2S4、Mo2C及Mo2C/ZnIn2S4样品的吸光性能进行了分析。图3(a)为材料的UV-vis DRS谱图。由图可知,纯ZnIn2S4的吸收带边约为514 nm,经Mo2C修饰后的Mo2C/ZnIn2S4复合材料对可见光的吸收有了明显的增强。随着Mo2C的增加,复合材料样品在紫外-可见光区的吸收强度和范围均逐渐增强。而Mo2C在整个吸收波段都表现出较强的吸收强度,这是由于Mo2C具有类金属的特性所导致的[15]。图3(b)为ZnIn2S4的Kubelka-Munk函数变换光谱,根据Kubellka-Munk公式(1)计算可得ZnIn2S4的Eg为2.41 eV。

图3 (a)紫外可见漫反射吸收光谱;
(b) ZnIn2S4的Kubelka-Munk函数变换光谱;
(c) ZnIn2S4的价带谱;
(d) Mo2C的价带谱Figure 3 Ultraviolet visible diffuse reflectance absorption spectrum (a), Kubelka-Munk function transform spectrum of ZnIn2S4 (b) and valence band spectrum of ZnIn2S4 (c) and Mo2C (d)

式中,hν、α、A和Eg分别代表光能,紫外可见漫反射的吸收指数、紫外可见漫反射的吸光度、禁带宽度。n代表半导体的类型,直接半导体n= 1,间接半导体n= 4,ZnIn2S4为直接半导体n= 1。
图3(c)为ZnIn2S4在XPS中测的价带谱,可得其价带电位为1.5 eV。由此可以算出ZnIn2S4的导带电位为-0.91 eV。同样,根据Mo2C的价带谱图(图3(d)),可以求得Mo2C的价带电位为-0.50 eV。由于金属导体的价带和导电位置相重合,所以价带和导带均为负值,这是由金属导体的自身原子组合方式所决定的。Mo2C的价带电位为负,说明Mo2C具有金属导体的性质,这可能是因为碳化钼的d带电子态密度与贵金属非常相似,具有类金属的特性,因此,展现出优异的导电性和光吸收特性[16]。当半导体和Mo2C复合后,两者之间存在界面电势差,会使它们之间形成类肖特基结。类肖特基结的形成有利于光催化剂载流子的分离与传输,有效提高光催化剂的催化活性。
2.1.4 XPS谱分析
X射线光电子能谱分析了材料表面元素及电子态,如图4所示。图4(a)为Mo2C和Mo2C/ZnIn2S4的全谱扫描,由全谱图可见,Mo2C/ZnIn2S4样品中存在Zn、In、S和C四种元素,由于Mo含量较低,分散性较强,所以信号较弱,所以导致其在全谱中未显示。此外,少量氧的O 1s峰为表面吸附的水或二氧化碳中氧原子信号[21]。图4(b)为样品Mo 3d高分辨谱图,Mo2C 谱图中228.6和231.8 eV处的峰对应Mo2+的3d5/2和 3d3/2轨道结合能,而232.8和235.9 eV处的弱峰对应Mo6+轨道结合能,这可能是由于材料表面Mo2+被部分氧化所致[22]。对于Mo2C/ZnIn2S4复合样品,在226.0 eV处的强峰对应ZnIn2S4中S 2s轨道结合能。在228.4eV处弱峰对应Mo2+3d5/2轨道结合能,谱峰信号较弱主要是由于附近S 2s轨道峰非常强,加之复合样品表面Mo含量较少和分散度较高所致[23]。图4(c)为Mo2C和Mo2C/ZnIn2S4中C 1s高分辨谱图,对比复合前后样品可以发现,复合后C 1s结合能向低结合能方向偏移0.2 eV(由284.95偏移到284.75 eV),而图4(d)和(e)中Zn 2p和In 3d轨道结合能向高结合能方向偏移0.4和0.3 eV,主要是由于在材料两相界面处物质相互作用,导致Zn和Mo原子周围的化学环境改变所引起。同时,C、Zn和In结合能的变化说明样品复合后,两相界面处电子密度发生重新分布。由于Mo2C的类金属特性,电负性大于ZnIn2S4,电子向Mo2C方向转移,C周围电子密度增大,因此,C 1s的结合能减小(负移),而Zn和In周围电子密度减小,故Zn 2p和In 3d电子结合能增大(正移)[24,25]。从全谱和精细谱均未发现N原子谱峰,说明原料中N元素在高温条件下分解并以气态形式挥发。用ICP发射光谱仪测得样品中Zn、In和Mo金属原子含量分别为13.91%、48.83%和9.41%。基本与投料比吻合,说明在水热条件下,硝酸锌,硝酸铟和硫代乙酰胺基本按化学计量比完全反应。
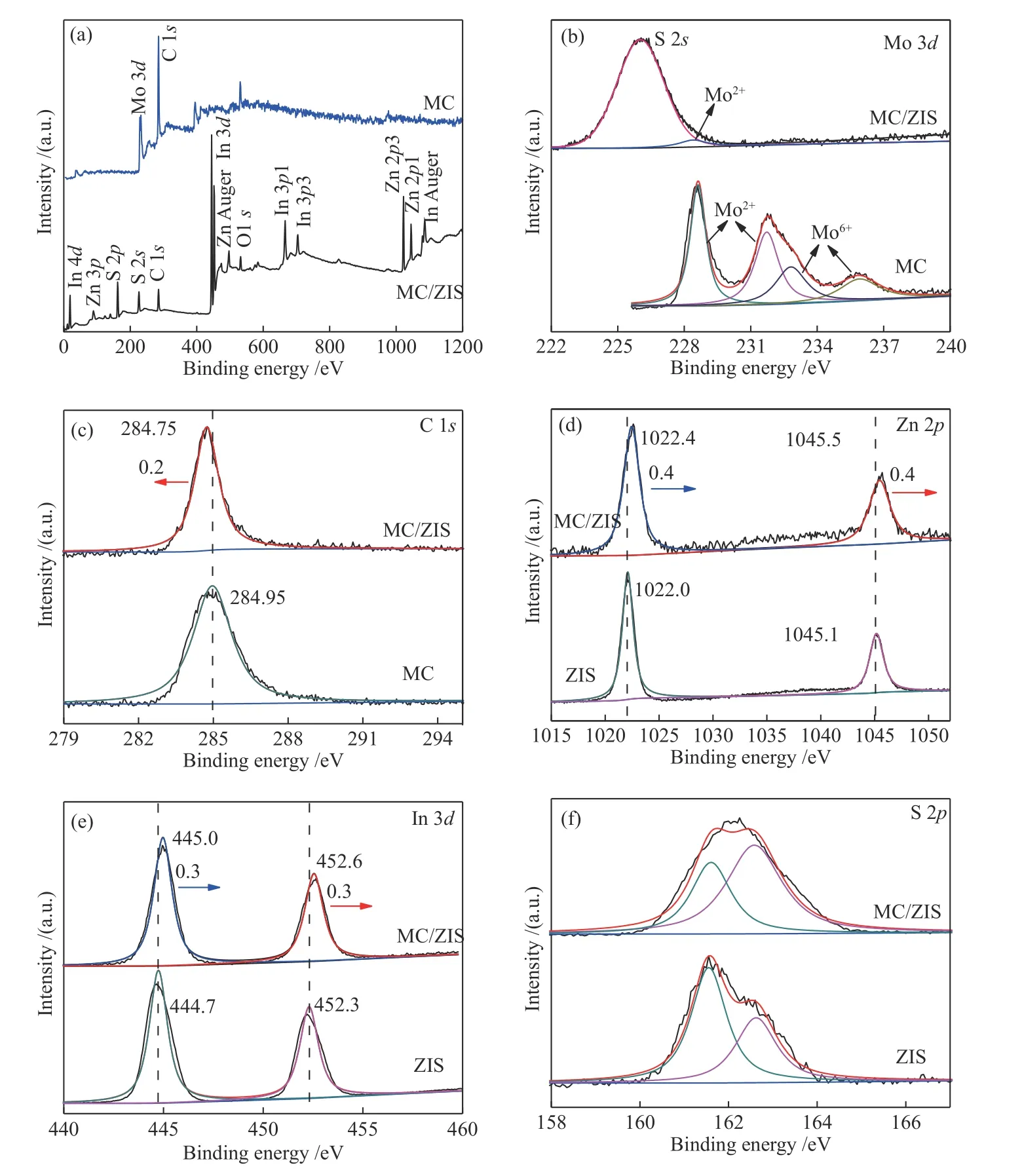
图4 样品XPS能谱图Figure 4 XPS spectra of survey (a), Mo 3d (b), C 1s (c) for Mo2C and Mo2C/ZnIn2S4, Zn 2p (d) and In 3d (e),In 3d and S 2p (f) for ZnIn2S4和Mo2C/ZnIn2S4
2.2 光催化剂光电性能分析
分别通过电化学测试和荧光测试研究了ZnIn2S4被Mo2C修饰前后电化学性质和光生载流子分离情况(图5)。由图5(a)可以看出,经Mo2C修饰后ZnIn2S4光电流响应明显增加,说明Mo2C修饰可以有效促进ZnIn2S4光生电荷的快速迁移,从而提了ZnIn2S4的载流子分离效率。图5(b)为Mo2C和Mo2C/ZnIn2S4的电化学阻抗图。一般来说,阻抗图中圆弧半径越大,相应的电化学阻抗也越大[26]。ZnIn2S4具有更大的圆弧半径,意味着具有更大的电化学阻抗,不利于自由电子的快速迁移。经过Mo2C修饰后,Mo2C/ZnIn2S4复合样品的电化学阻抗明显降低,这主要由于碳化钼具有优异的导电性,可以有效的促进载流子的快速迁移,从而提高复合样品的光催化活性。图5(c)为Mo2C和Mo2C/ZnIn2S4的荧光光谱。从图5(c)可以看出,经Mo2C修饰后,Mo2C/ZnIn2S4复合样品荧光强度明显降低,说明Mo2C的修饰可以有效抑制ZnIn2S4光生载流子的复合,有利于其光催化活性的提高[27]。同时发现,Mo2C/ZnIn2S4荧光峰位相对于ZnIn2S4纯样峰位发生蓝移,这主要是由于Mo2C和ZnIn2S4形成异质结复合材料所致[28]。图5(d)为Mo2C和Mo2C/ZnIn2S4的线性扫描伏安曲线(LSV),LSV曲线可以反映材料在析氢反应过程中过电势的高低[29]。从图5(d)可以看出,ZnIn2S4纯样和Mo2C/ZnIn2S4复合样品在达到相同的电流密度时,复合样品的过电势更低,意味着在Mo2C/ZnIn2S4表面更容易发生析氢反应。

图5 (a) ZIS和MC/ZIS的瞬态光电流响应谱图;
(b) EIS谱图;
(c) PL谱图;
(d) LSV曲线Figure 5 Transient photocurrent response spectra (a), EIS specta (b) ,PL spectra (c) and LSV curves (d) of ZIS and MC/ZIS
2.3 光催化析氢性能
在可见光条件下对所制备的ZnIn2S4和Mo2C/ZnIn2S4样品进行了光催化析氢测试和重复性试验(图6)。如图6(a)所示, ZnIn2S4纯样的析氢速率为0.26 mmol/(g·h),Mo2C本身几乎无任何活性,而Mo2C/ZnIn2S4复合样品析氢活性明显高于ZnIn2S4纯样,且随复合样中Mo2C含量的增加,复合样品析氢活性有显著提高。当含量为10%时,样品析氢活性达到最大,析氢速率约为1.33 mmol/(g·h),与ZnIn2S4纯样相比提高了约4.1倍。再增加Mo2C的含量,析氢活性反而下降,主要是由于当Mo2C的加入量较少时,有效的活性位点相应较少,因此,限制了光催化析氢效率的提高。随着Mo2C含量的增加,有效的活性位点也在不断增加,载流子分离效率不断提高,从而提高复合光催化剂的析氢效率。但当Mo2C含量过高时,ZnIn2S4表面负载过多Mo2C会影响催化剂对光的有效吸收,导致光催化活性的降低。此外,如前所述由于碳化钼具有类金属的特性,展现出优异的光吸收特性,吸收的部分光可能为转变为热能。因此,为了尽可能避免助催化剂热效应对催化活性的影响,在光催化反应体系中使用循环水冷却系统,使反应体系温度尽量保持在20 ℃的恒温环境。10%Mo2C/ZnIn2S4复合样品光催化循环析氢稳定性实验显示,经过五次循环析氢实验后的Mo2C/ZnIn2S4复合光催化剂仍表现出稳定的光催化析氢活性(图6(b))说明所制备的Mo2C/ZnIn2S4复合光催化剂具有良好的光催化稳定性。
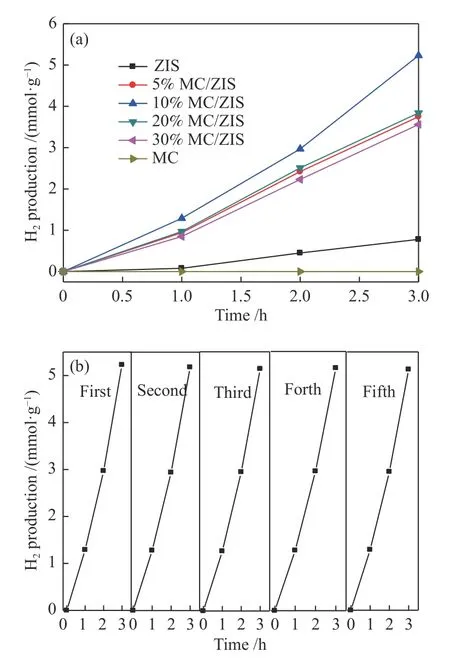
图6 (a) 不同Mo2C负载量MC/ZIS产氢速率,(b) 10%MC/ZIS的光催化产氢循环实验Figure 6 MC/ZIS hydrogen production diagram (a) with different loading of Mo2C and 10% MC/ZIS photocatalytic hydrogen production cycle experiment diagram (b)
2.4 光催化机理分析
为进一步研究Mo2C/ZnIn2S4复合光催化剂的电子转移机理,使用开尔文探针分别测量了Mo2C和ZnIn2S4样品的表面功函。以Au为参比,得到Mo2C和ZnIn2S4的相对接触电势差,结果如图7所示。通过公式(2)[30]分别计算得到Mo2C和ZnIn2S4的表面功函分别为WF(ZIS) = 4.87 eV、WF(MC) =5.29 eV。

图7 ZIS和MC的功函谱图Figure 7 Work function maps of ZIS and MC
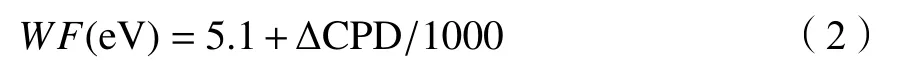
基于上述实验和计算结果,推断了Mo2C在ZnIn2S4光催化析氢反应中的作用机制(图8):在原位复合过程中,Mo2C和ZnIn2S4之间构建了紧密的异质界面。在可见光照射下,ZnIn2S4可以产生大量的光生电子和空穴。由于Mo2C具有比ZnIn2S4更低的表面功函,当两者接触时,它们之间的功函差会导致ZnIn2S4的电子向Mo2C流动,从而形成由ZnIn2S4指向Mo2C的内建电场。在光催化析氢过程中,光生电子在内建电场的驱动下快速转移至Mo2C和ZnIn2S4的异质界面处。同时,由于Mo2C较高的导电性和较低的析氢过电位,使光生电子快速迁移至Mo2C表面,并使表面吸附的H+发生还原反应。整个过程中,Mo2C的存在明显增强了ZnIn2S4光生载流子的分离效率,降低了表面光催化析氢反应的过电位,从而实现了高效率的光催化分解水析氢。
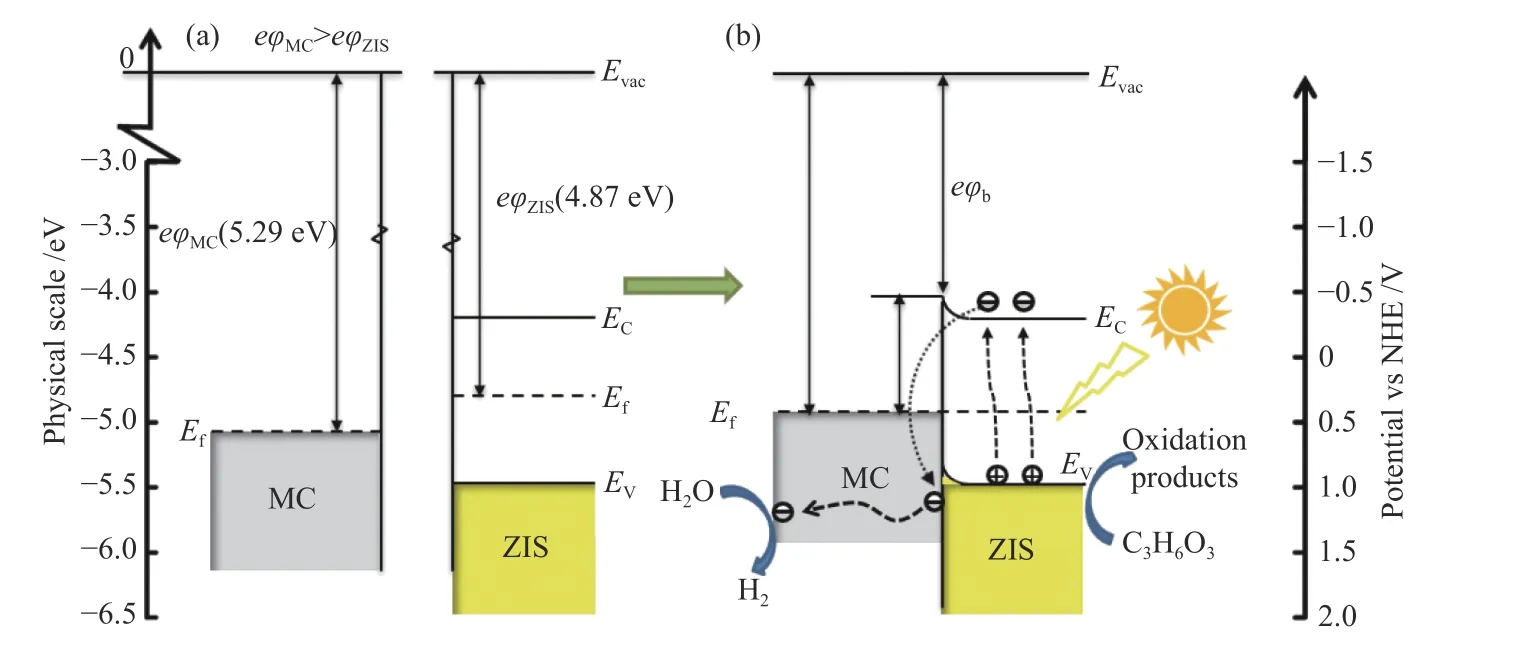
图8 Mo2C/ZnIn2S4 复合光催化剂的光催化析氢机制Figure 8 Photocatalytic hydrogen evolution mechanism of Mo2C/ZnIn2S4 composite photocatalyst
本研究采用高温固相法合成了Mo2C纳米粒子,然后通过原位水热法制备了Mo2C/ZnIn2S4复合光催化剂。通过调控两者之间的连结界面形成了稳定高效的复合光催化材料。当合成过程中加入的钼酸铵与二氰二胺的质量比为1∶2,Mo2C/ZnIn2S4复合材料中Mo2C负载量为10%时,复合材料表现出显著增强的光催化活,其光解水析氢速 率 为1.33 mmol/(g·h),约为纯ZnIn2S4的5.1倍。光催化活性增强机制可归结为:具有类金属性的Mo2C修饰ZnIn2S4形成有效异质界面,界面处产生内建电场,增强了光生电荷的分离和传输效率。同时由于Mo2C较低的析氢过电位,复合材料光催化析氢效率得到显著提升。
猜你喜欢 光催化剂光催化复合材料 过渡金属硫化物基复合光催化剂制备及其性能研究*化学与粘合(2022年5期)2022-10-31夹芯复合材料加筋板真空和水中自由振动分析舰船科学技术(2022年11期)2022-07-15浅谈现代建筑中新型复合材料的应用建材发展导向(2022年2期)2022-03-08Marvelous mural 神奇的壁画疯狂英语·新阅版(2021年9期)2021-10-30中国科学技术大学研制出新型高效硫化物光催化剂科学导报(2020年70期)2020-11-09国产复合材料预浸料过程控制的认识与实践民用飞机设计与研究(2020年1期)2020-05-21先进复合材料制造及过程控制技术民用飞机设计与研究(2020年1期)2020-05-21光催化剂能用可见光分解水科学导报(2019年42期)2019-09-03半导体光催化材料钨酸铋的研究进展中国科技纵横(2019年3期)2019-03-25二氧化钛光催化产生超氧自由基的形态分布研究分析化学(2017年12期)2017-12-25








